高中 | 化学平衡移动及其影响因素 题目答案及解析
稿件来源:高途
高中 | 化学平衡移动及其影响因素题目答案及解析如下,仅供参考!
选修四
第二章 化学反应速率和化学平衡
第三节 化学平衡
化学平衡移动及其影响因素
乙烯工业是石油化工产业的核心,在国民经济中占有重要的地位。生活中,乙烯也是一种常见的水果催熟剂。乙烯能发生如下图所示的化学变化,其中化合物$\rm D$是一种具有香味的液体,物质$\rm E$是常见的高分子材料。
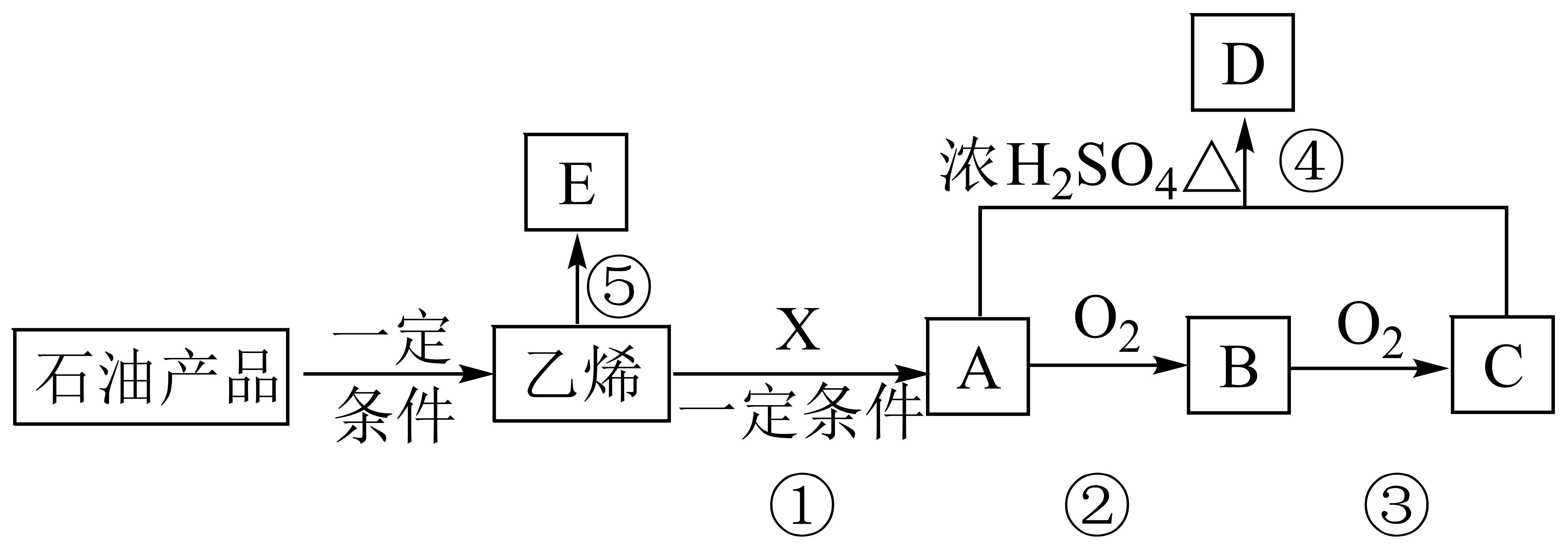
乙烯的结构式为 ,其中$\rm \pi$键与$\rm \sigma$键的数目比为 。
$\\rm CH_{2}=CH_{2}$ ;$\\rm 1: 5$
"]]乙烯的分子式为$\rm C_{2}H_{4}$,官能团为碳碳双键,结构简式为$\rm CH_{2}=CH_{2}$,乙烯分子中单键为$\rm \sigma$键,双键中含有$\rm 1$个$\rm \sigma$键和$\rm 1$个$\rm \pi$键,则分子中$\rm \pi$键与$\rm \sigma$键的数目比为$\rm 1$:$\rm 5$;
在水果箱中放入一些用$\rm 0.2\%$的高锰酸钾溶液浸泡过的纸,封严水果箱,能延长水果的保质期,说明其中的化学原理 。
高锰酸钾溶液吸收水果释放出的乙烯
"]]水果能释放乙烯促进水果的成熟,所以在水果箱中放入一些用$\rm 0.2\%$的高锰酸钾溶液浸泡过的纸,封严水果箱,可以用高锰酸钾溶液吸收乙烯,延长水果的保质期;
反应①中无机物$\rm X$为 ,反应①的类型为 反应。
$\\rm H_{2}O$; 加成
"]]由分析可知,反应①为一定条件下乙烯与水发生加成反应生成乙醇,则无机物$\rm X$为水;
反应②的方程式为 。
$\\rm 2CH_{3}CH_{2}OH+O_{2}\\xrightarrow[加热]{\\text{Cu}}2CH_{3}CHO+2H_{2}O$
"]]由分析可知,反应②为铜做催化剂条件下乙醇与氧气共热发生催化氧化反应生成乙醛,反应的化学方程式为$\rm 2CH_{3}CH_{2}OH+O_{2}\xrightarrow[加热]{\text{Cu}}2CH_{3}CHO+2H_{2}O$;
以下关于物质$\rm E$的表述,正确的是$(\quad\ \ \ \ )$。$\rm ($复选$\rm )$
物质$\\rm E$为纯净物
","物质$\\rm E$不能使溴水褪色
","物质$\\rm E$中所有碳原子共平面
","反应⑤为熵减过程,却能自发进行,可知该反应的$\\Delta H\\lt 0$
"]$\rm A$.聚乙烯分子中的聚合度$n$值为不确定值,所以聚乙烯属于混合物,故错误;
$\rm B$.聚乙烯分子中不含有碳碳双键,不能与溴水发生加成反应使溶液褪色,故正确;
$\rm C$.聚乙烯分子中的碳原子都是空间构型为四面体形的饱和碳原子,所以分子中所有碳原子不可能共平面,故错误;
$\rm D$.反应⑤为一定条件下,乙烯发生加聚反应生成聚乙烯,反应为熵减过程,反应能自发进行,说明反应$ \Delta H-T\Delta S\lt 0$,则反应的焓变小于$\rm 0$,故正确;
故选:$\rm BD$;
下图是实验室制备$\rm D$的装置示意图:
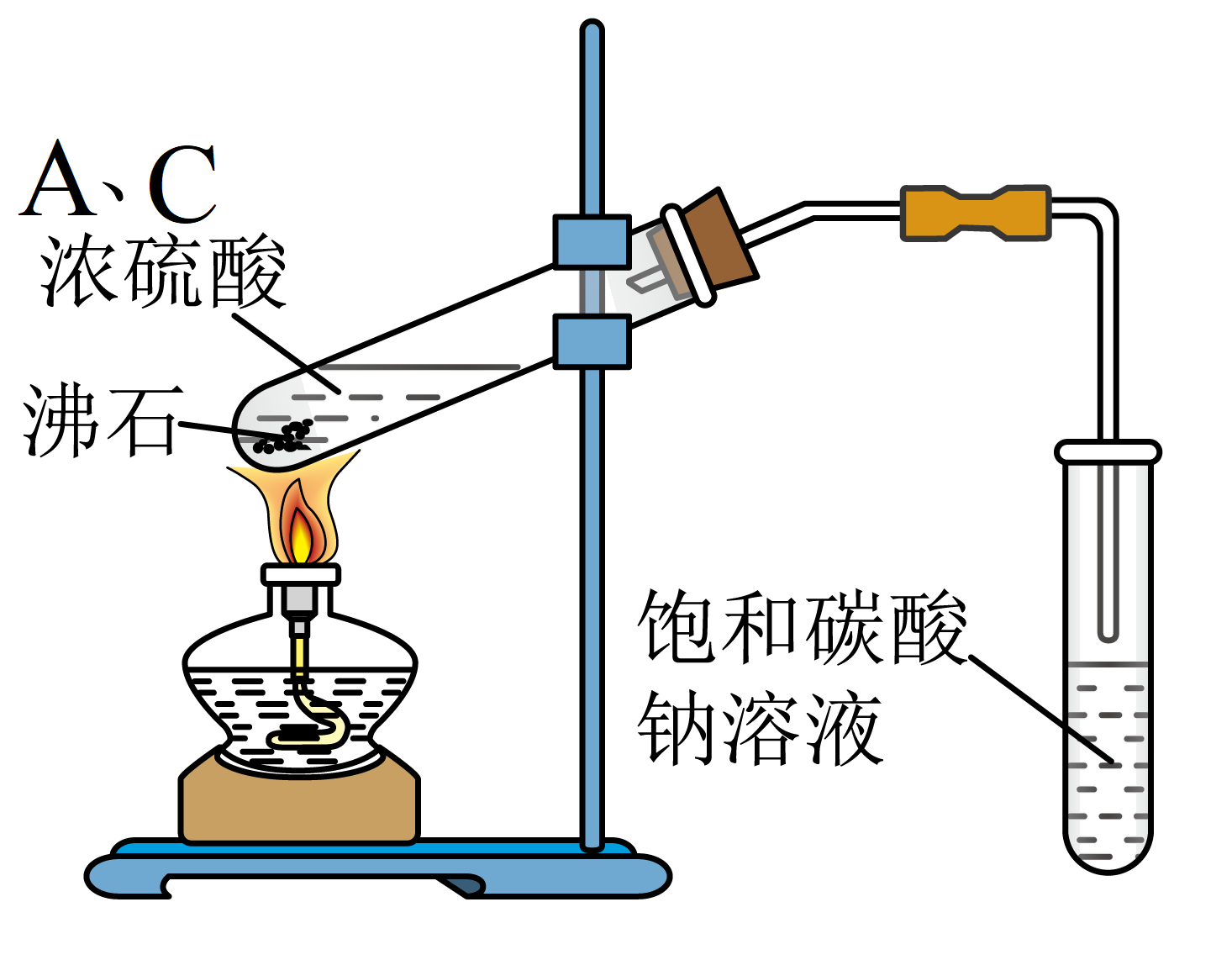
从反应后的混合物中分离得到$\rm D$,应选择的分离方法为$(\quad\ \ \ \ )$。
过滤
","渗析
","分液
","蒸馏
"]乙酸乙酯不溶于水,则从饱和碳酸钠溶液中分离出乙酸乙酯的操作为分液;
物质$\rm D$的同分异构体$\rm ($不包含物质$\rm D)$中属于酯类的数目有$(\quad\ \ \ \ )$种。
$\\rm 1$
","$\\rm 2$
","$\\rm 3$
","$\\rm 4$
"]乙酸乙酯的同分异构体中属于酯类的有机物为丙酸甲酯、甲酸$\rm -1-$丙酯、甲酸$\rm-2-$丙酯,共有$\rm 3$种;
为了提高$\rm C$的转化率,采取的措施有 、 $\rm ($写两条$\rm )$。
加入过量的$\\rm CH_{3}CH_{2}OH$ ;分离出$\\rm CH_{3}COOCH_{2}CH_{3}$
"]]加入过量的乙醇、分离出乙酸乙酯的措施,都能使平衡向正反应方向移动,有利于提高乙酸的转化率,故:加入过量的$\rm CH_{3}CH_{2}OH$;分离出$\rm CH_{3}COOCH_{2}CH_{3}$。
高中 | 化学平衡移动及其影响因素题目答案及解析(完整版)
