高中 | 杂化轨道理论 题目答案及解析
稿件来源:高途
高中 | 杂化轨道理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
杂化轨道理论
$\rm Be$及其化合物的转化关系如图。下列说法错误的是$(\qquad)$
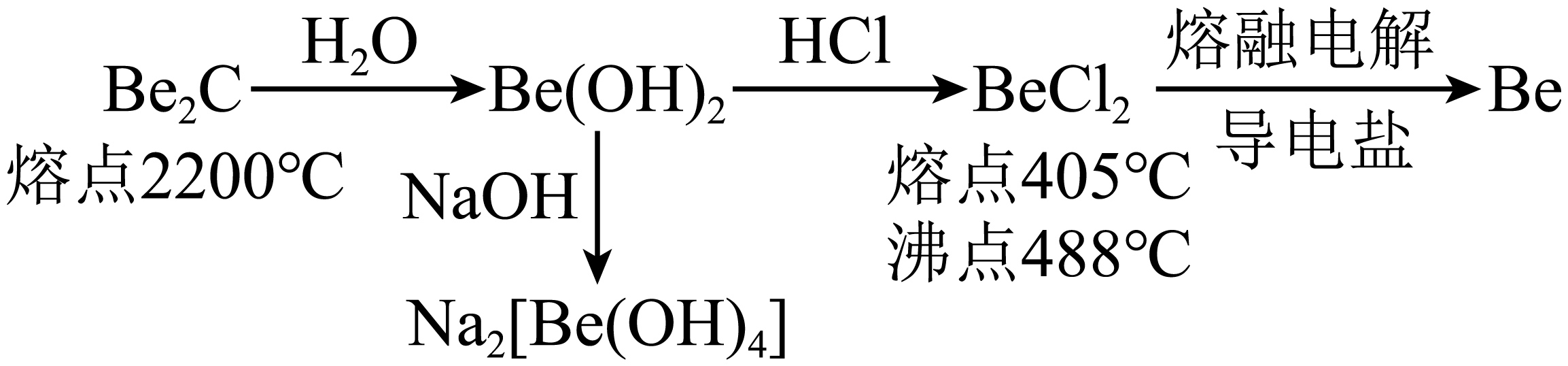
$\\text{Be}{{\\left( \\text{OH} \\right)}_{2}}$是两性氢氧化物
","$\\text{B}{{\\text{e}}_{2}}\\text{C}$和$\\text{BeC}{{\\text{l}}_{2}}$的晶体类型相同
","$\\text{N}{{\\text{a}}_{2}}\\left[ \\text{Be}{{\\left( \\text{OH} \\right)}_{4}} \\right]$中$\\rm Be$原子的杂化方式为$\\text{s}{{\\text{p}}^{3}}$
","$\\text{B}{{\\text{e}}_{2}}\\text{C}$与${{\\text{H}}_{2}}\\text{O}$反应:$\\text{B}{{\\text{e}}_{2}}\\text{C}+4{{\\text{H}}_{2}}\\text{O}=2\\text{Be}{{\\left( \\text{OH} \\right)}_{2}}+\\text{C}{{\\text{H}}_{4}}\\uparrow $
"]$\rm A$.由图中转化信息可知,$\text{Be}{{\left( \text{OH} \right)}_{2}}$既能与盐酸反应生成盐和水,又能与氢氧化钠反应生成盐,因此其是两性氢氧化物,$\rm A$正确;
$\rm B$.由题中信息可知,$\text{B}{{\text{e}}_{2}}\text{C}$的熔点远远高于$\text{BeC}{{\text{l}}_{2}}$的,因此$\text{B}{{\text{e}}_{2}}\text{C}$不可能是分子晶体,而$\text{BeC}{{\text{l}}_{2}}$的熔点和沸点均较低,其为分子晶体,因此两者的晶体类型不相同,$\rm B$错误;
$\rm C$.$\text{N}{{\text{a}}_{2}}\left[ \text{Be}{{\left( \text{OH} \right)}_{4}} \right]$中 $\rm Be$ 原子与$\rm 4$个羟基形成$\rm 4$个$\rm \sigma$键,没有孤电子对,只有$\rm 4$个成键电子对,因此,其杂化方式为 $\rm sp^{3}$,$\rm C$正确;
$\rm D$.$\text{B}{{\text{e}}_{2}}\text{C}$中的$\rm Be$化合价为$\rm +2$,$\rm C$的化合价为$\rm -4$,因此其与${{\text{H}}_{2}}\text{O}$反应生成$\text{Be}{{\left( \text{OH} \right)}_{2}}$和$\text{C}{{\text{H}}_{4}}$,该反应的化学方程式为$\text{B}{{\text{e}}_{2}}\text{C}+4{{\text{H}}_{2}}\text{O}=2\text{Be}{{\left( \text{OH} \right)}_{2}}+\text{C}{{\text{H}}_{4}}\uparrow $,$\rm D$正确;
故选:$\rm B$
高中 | 杂化轨道理论题目答案及解析(完整版)
