| 盐类水解常数 题目答案及解析
稿件来源:高途
| 盐类水解常数题目答案及解析如下,仅供参考!
选修四
第三章 水溶液中的离子平衡
第三节 盐类的水解
盐类水解常数
氨基乙酸$\left( \text{N}{{\text{H}}_{2}}\text{C}{{\text{H}}_{2}}\text{COOH} \right)$是结构最简单的氨基酸分子,其分子在水溶液中存在如下平衡:
$^{*}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{COOH} \overset{{\rm p}K_1=2.4 }{\underset{ }{\rightleftharpoons}} \text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}} \overset{{\rm p}K_2=9.6 }{\underset{ }{\rightleftharpoons}} \text{N}{{\text{H}}_{2}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}}$
在$\rm 25\;\rm ^\circ\rm C$时,其分布分数$\delta\rm [$如$\delta { \rm(N}{{\text{H}}_{2}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}}) =\dfrac{c\text{(N}{{\text{H}}_{2}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}})}{{c}{{\text{(}}^{*}}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{COOH})+{c}{{\text{(}}^{*}}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}})+c\text{(N}{{\text{H}}_{2}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}})}\rm ]$
与溶液$\rm pH$关系如图$\rm 1$所示。在$100\;\rm \text{mL}\;\rm 0.01\;\rm \text{mol}/{{\text{L }}^{*}}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{COOH}\cdot \text{C}{{\text{l}}^{-}}$溶液中逐滴滴入$\rm 0.1\;\rm mol/L\;NaOH$溶液,溶液$\rm pH$与$\rm NaOH$溶液滴入体积的变化关系如图$\rm 2$所示。下列说法错误的是$(\qquad)$
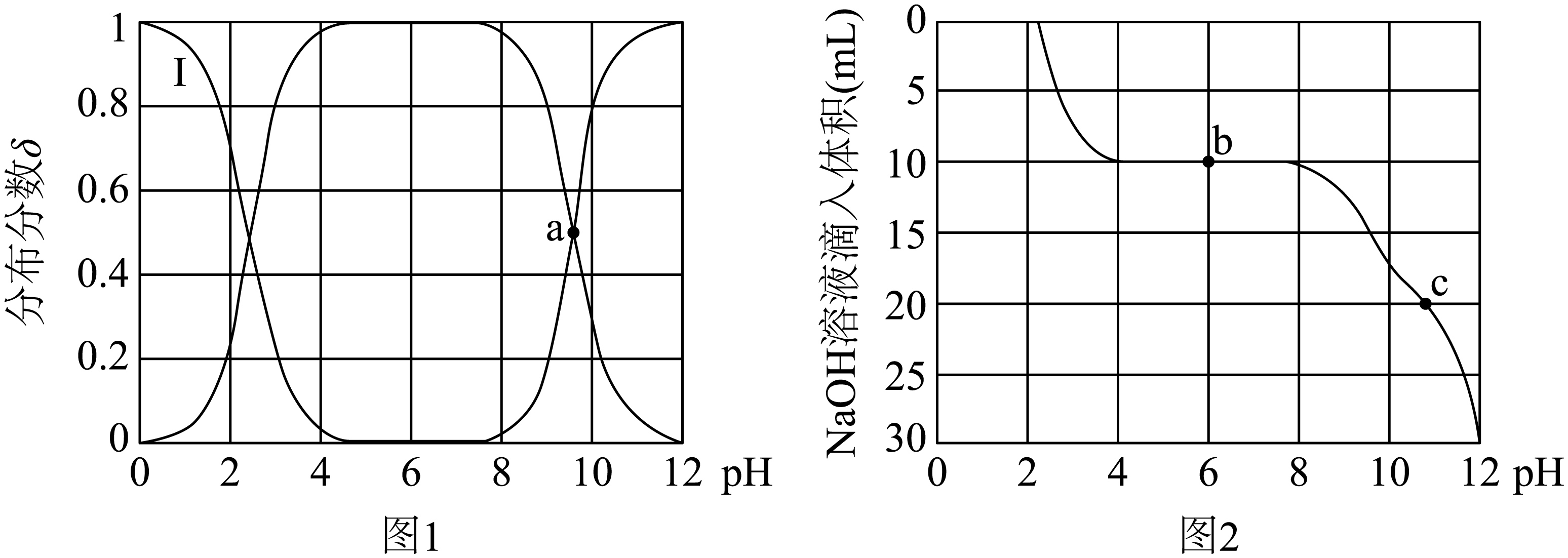
曲线Ⅰ对应的离子是$\\rm ^{*}\\text{N}{{\\text{H}}_{3}}\\text{C}{{\\text{H}}_{2}}\\text{COOH}$
","$\\rm a$点处对应的$\\rm pH$为$\\rm 9.6$
","$\\rm b$点处${c}\\left( ^{*}\\text{N}{{\\text{H}}_{3}}\\text{C}{{\\text{H}}_{2}}\\text{COOH} \\right)={c}\\left( \\text{N}{{\\text{H}}_{2}}\\text{C}{{\\text{H}}_{2}}\\text{CO}{{\\text{O}}^{-}} \\right)$
","$\\rm c$点处$2{c}\\left( ^{*}\\text{N}{{\\text{H}}_{3}}\\text{C}{{\\text{H}}_{2}}\\text{COOH} \\right)+{c}\\left( ^{*}\\text{N}{{\\text{H}}_{3}}\\text{C}{{\\text{H}}_{2}}\\text{CO}{{\\text{O}}^{-}} \\right)+{c}\\left( {{\\text{H}}^{\\text{*}}} \\right)={c}\\left( \\text{O}{{\\text{H}}^{-}} \\right)$
"]图$\rm 1$可知,随着$\rm pH$增大,平衡$^{*}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{COOH} \overset{{\rm p}K_1=2.4 }{\underset{ }{\rightleftharpoons}} \text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}} \overset{{\rm p}K_2=9.6 }{\underset{ }{\rightleftharpoons}} \text{N}{{\text{H}}_{2}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}}$右移,$\rm ^{*\rm }NH_{3}CH_{2}COOH$的分布分数减少,$\rm NH_{3}CH_{2}COO^{-}$先增加后减少,$\rm NH_{2}CH_{2}COO^{-}$最后增加,$\rm a$点代表$\rm NH_{3}CH_{2}COO^{-}$和$\rm NH_{2}CH_{2}COO^{-}$分布分数相等的点;图$\rm 2$中$\rm b$点滴入$\rm NaOH$为$\rm 10\;\rm mL$,$\rm ^{*}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{COOH}\cdot \text{C}{{\text{l}}^{-}}$和$\rm NaOH$的物质的量相等,得到$\rm NH_{3}CH_{2}COO^{-}$,$\rm c$点$\rm ^{*}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{COOH}\cdot \text{C}{{\text{l}}^{-}}$和$\rm NaOH$的物质的量之比为$\rm 1:2$,得到主要粒子为$\rm NH_{2}CH_{2}COO^{-}$。
$\rm A$.根据分析可知,随着$\rm pH$值增大,$\rm ^{*\rm }NH_{3}CH_{2}COOH$的分布分数减少,曲线$\rm I$代表$\rm ^{*\rm }NH_{3}CH_{2}COOH$的分布分数,$\rm A$正确;
$\rm B$.$\rm a$点代表$\rm NH_{3}CH_{2}COO^{-}$和$\rm NH_{2}CH_{2}COO^{-}$分布分数相等的点,二者浓度相等,$ \rm P k\rm _{a2}=9.6$,$ K_{\rm a2}=\dfrac{{c}\left( \text{N}{{\text{H}}_{2}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}} \right)\times {c}\left( {{\text{H}}^{+}} \right)}{{c}(\left( \text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}} \right)}={c}\left( {{\text{H}}^{+}} \right)={{10}^{-9.6}}$,$\rm pH=9.6$,$\rm B$正确;
$\rm C$.图$\rm 2$中$\rm b$点滴入$\rm NaOH$为$\rm 10\;\rm mL$,$^{*}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{COOH}\cdot \text{C}{{\text{l}}^{-}}$和$\rm NaOH$的物质的量相等,得到主要离子为$\rm NH_{3}CH_{2}COO^{-}$,$\rm NH_{3}CH_{2}COO^{-}$存在电离和水解,$K_{\rm a2}=10^{-9.6}$,$K_{\rm h}=\dfrac{{{ {K}}_{\text{w}}}}{{{ {K}}_{\text{a}1}}}\rm =\dfrac{{{10}^{-14}}}{{{10}^{-2.4}}}={{10}^{-11.6}}$,电离大于水解,则${c}\left( ^{*}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{COOH} \right)\lt {c}\left( \text{N}{{\text{H}}_{2}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}} \right)$,$\rm C$错误;
$\rm D$.$\rm c$点$^{*}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{COOH}\cdot \text{C}{{\text{l}}^{-}}$和$\rm NaOH$的物质的量之比为$\rm 1:2$,得到主要粒子为$\rm NH_{2}CH_{2}COO^{-}$,根据质子守恒,有$2{c}\left( ^{*}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{COOH} \right)+{c}\left( ^{*}\text{N}{{\text{H}}_{3}}\text{C}{{\text{H}}_{2}}\text{CO}{{\text{O}}^{-}} \right)+{c}\left( {{\text{H}}^{\text{*}}} \right)={c}\left( \text{O}{{\text{H}}^{-}} \right)$,$\rm D$正确。
故选:$\rm C$
| 盐类水解常数题目答案及解析(完整版)
