高中 | 配合物理论 题目答案及解析
稿件来源:高途
高中 | 配合物理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
配合物理论
实验室从$\rm AgCl$中提取$\rm Ag$的一种实验方案如下:
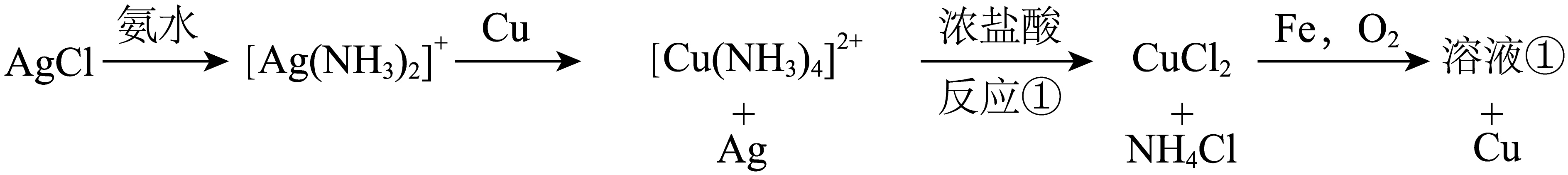
下列说法错误的是$(\quad\ \ \ \ )$
还原性:$\\rm Fe\\gt Cu\\gt Ag$
","${{\\left[ \\text{Ag}{{\\left( \\text{N}{{\\text{H}}_{3}} \\right)}_{2}} \\right]}^{+}}$、${{\\left[ \\text{Cu}{{\\left( \\text{N}{{\\text{H}}_{3}} \\right)}_{4}} \\right]}^{2+}}$中的中心离子的配位数分别为$\\rm 2$、$\\rm 4$
","反应①的离子方程式是${{\\left[ \\text{Cu}{{\\left( \\text{N}{{\\text{H}}_{3}} \\right)}_{4}} \\right]}^{2+}}+4{{\\text{H}}^{+}}=\\text{C}{{\\text{u}}^{2+}}+4\\text{NH}_{4}^{+}$
","溶液①中的金属离子是$\\text{F}{{\\text{e}}^{2+}}$
"]$\rm AgCl$与氨水反应生成${{\left[ \text{Ag}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{2}} \right]}^{+}}$,${{\left[ \text{Ag}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{2}} \right]}^{+}}$与$\rm Cu$反应生成${{\left[ \text{Cu}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}} \right]}^{2+}}$和$\rm Ag$,${{\left[ \text{Cu}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}} \right]}^{2+}}$中加入浓盐酸,发生$\left[ \text{Cu}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}} \right]\text{C}{{\text{l}}_{2}}+4\text{HCl}=\text{CuC}{{\text{l}}_{2}}+4\text{N}{{\text{H}}_{4}}\text{Cl}$,生成$\text{CuC}{{\text{l}}_{2}}$,向氯化铜和氯化铵的混合液中加入单质铁,铁置换出铜后生成$\text{F}{{\text{e}}^{2+}}$,然后$\text{F}{{\text{e}}^{2+}}$被通入的氧气氧化为$\text{F}{{\text{e}}^{3+}}$,据此回答。
$\rm A$.金属活动性越强,金属的还原性越强,而且由题中的实验方案能得到证明,还原性由强到弱的顺序为$\rm Fe\gt Cu\gt Ag$,$\rm A$正确;
$\rm B$.${{\left[ \text{Ag}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{2}} \right]}^{+}}$、${{\left[ \text{Cu}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}} \right]}^{2+}}$中的中心离子的配位数分别为$\rm 2$、$\rm 4$,$\rm B$正确;
$\rm C$.反应①中,氯化四氨合铜溶液与浓盐酸反应生成氯化铜和氯化铵,该反应的离子方程式是${{\left[ \text{Cu}{{\left( \text{N}{{\text{H}}_{3}} \right)}_{4}} \right]}^{2+}}+4{{\text{H}}^{+}}=\text{C}{{\text{u}}^{2+}}+4\text{NH}_{4}^{+}$,$\rm C$正确;
$\rm D$.向氯化铜和氯化铵的混合液中加入单质铁,铁置换出铜后生成$\text{F}{{\text{e}}^{2+}}$,然后$\text{F}{{\text{e}}^{2+}}$被通入的氧气氧化为$\text{F}{{\text{e}}^{3+}}$,因此,溶液①中的金属离子是$\text{F}{{\text{e}}^{3+}}$,$\rm D$错误;
故选:$\rm D$
高中 | 配合物理论题目答案及解析(完整版)
