高中 | 氧化还原反应方程式的书写及配平 题目答案及解析
稿件来源:高途
高中 | 氧化还原反应方程式的书写及配平题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第三节 氧化还原反应
氧化还原反应方程式的书写及配平
$\text{B}{{\text{r}}_{2}}$具有较强的氧化性,能够将磷氧化为$\text{PB}{{\text{r}}_{3}}$或$\text{PB}{{\text{r}}_{5}}\rm (\text{PB}{{\text{r}}_{5}}$可以水解得到两种酸$\rm )$,与氨反应生成溴化铵和氮气,可以氧化一些非金属阴离子,如$\text{B}{{\text{r}}_{2}}$与${{\text{S}}^{2-}}$反应生成${{\text{S}}_{8}}\rm ($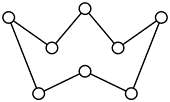 $\rm )$。在催化剂作用下,苯与$\text{B}{{\text{r}}_{2}}$发生取代反应,该反应属于放热反应。醛与$\text{B}{{\text{r}}_{2}}$在碱的催化下,醛的$\alpha-$氢被溴取代生成$\alpha-$溴代醛。工业上海水提溴的主要过程为:
$\rm )$。在催化剂作用下,苯与$\text{B}{{\text{r}}_{2}}$发生取代反应,该反应属于放热反应。醛与$\text{B}{{\text{r}}_{2}}$在碱的催化下,醛的$\alpha-$氢被溴取代生成$\alpha-$溴代醛。工业上海水提溴的主要过程为:![]()
下列化学用语表示正确的是$(\quad\ \ \ \ )$
$\\text{PB}{{\\text{r}}_{5}}$水解反应的化学方程式:$\\text{PB}{{\\text{r}}_{5}}+4{{\\text{H}}_{2}}\\text{O}={{\\text{H}}_{3}}\\text{P}{{\\text{O}}_{4}}+5\\text{HBrO}$
","溴与氨反应的化学方程式:$3\\text{B}{{\\text{r}}_{2}}+8\\text{N}{{\\text{H}}_{3}}=6\\text{N}{{\\text{H}}_{4}}\\text{Br}+{{\\text{N}}_{2}}$
","乙醛与溴反应生成$\\alpha-$溴代乙醛的化学方程式:$\\text{C}{{\\text{H}}_{3}}\\text{CHO}+\\text{B}{{\\text{r}}_{2}}\\xrightarrow{\\text{O}{{\\text{H}}^{-}}}$$+\\text{HBr}$
","纯碱溶液吸收$\\text{B}{{\\text{r}}_{2}}$的离子方程式:$\\text{B}{{\\text{r}}_{2}}+\\text{CO}_{3}^{2-}=\\text{B}{{\\text{r}}^{-}}+\\text{BrO}_{3}^{-}+\\text{C}{{\\text{O}}_{2}}\\uparrow $
"]$\rm A$.$\rm PBr_{5}$水解生成磷酸和氢溴酸,反应的化学方程式为:$\text{PB}{{\text{r}}_{5}}+4{{\text{H}}_{2}}\text{O}={{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}+5\text{HBr}$,$\rm A$错误;
$\rm B$.溴与氨反应生成溴化铵和氮气,反应的化学方程式为:$\rm 3Br_{2}+8NH_{3}=6NH_{4}Br+N_{2}$,$\rm B$正确;
$\rm C$.乙醛与溴发生取代反应生成$\rm \alpha$−溴代乙醛和氢溴酸,反应的化学方程式为:$\text{B}{{\text{r}}_{\text{2}}}+\text{C}{{\text{H}}_{\text{3}}}\text{CHO}\underset{\text{O}{{\text{H}}^{-}}}{\overset{催化剂}{\mathop{\to }}}\,\text{Br}-\text{C}{{\text{H}}_{\text{2}}}\text{CHO}+\text{HBr}$,$\rm C$错误;
$\rm D$.用纯碱溶液吸收$\rm Br_{2}$时,生成溴化钠、溴酸钠和碳酸氢钠,反应的离子方程式为:$\text{3B}{{\text{r}}_{\text{2}}}\text{+6CO}_{3}^{2-}\text{+3}{{\text{H}}_{\text{2}}}\text{O=5B}{{\text{r}}^{-}}\text{+BrO}_{3}^{-}\text{+6HCO}_{3}^{-}$,$\rm D$错误;
故选:$\rm B$
高中 | 氧化还原反应方程式的书写及配平题目答案及解析(完整版)
