高中 | 化学平衡常数 题目答案及解析
稿件来源:高途
高中 | 化学平衡常数题目答案及解析如下,仅供参考!
选修四
第二章 化学反应速率和化学平衡
第三节 化学平衡
化学平衡常数
反应$4\text{N}{{\text{H}}_{3}}\left( \text{g} \right)+4\text{NO}\left( \text{g} \right)+{{\text{O}}_{2}}\left( \text{g} \right)\rightleftharpoons 4{{\text{N}}_{2}}\left( \text{g} \right)+6{{\text{H}}_{2}}\text{O}\left( \text{g} \right)$可用于去除氮氧化物。有氧条件下,等物质的量的$\text{NO}$、$\text{N}{{\text{H}}_{3}}$在钒基催化剂$\mathrm{V}_{2} \mathrm{O}_{5}$作用下的反应机理如图所示。下列说法正确的是$(\quad\ \ \ \ )$
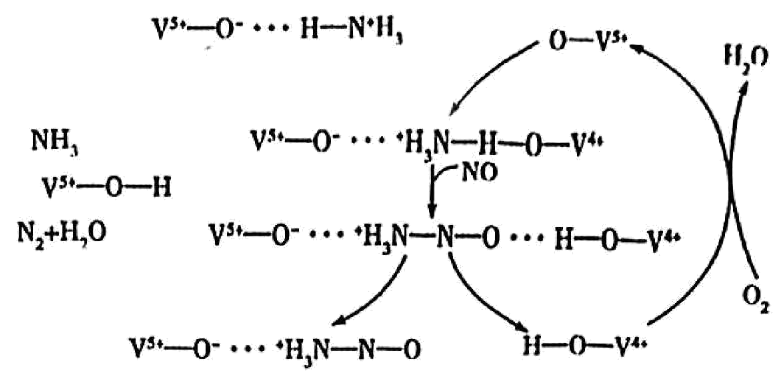
反应过程中,$\\mathrm{V}_{2} \\mathrm{O}_{5}$参与反应,降低了反应的焓变
","该反应的平衡常数$K=\\dfrac{{{c}^{4}}\\left( {{\\text{N}}_{2}} \\right)}{{{c}^{4}}\\left( \\text{N}{{\\text{H}}_{3}} \\right)\\cdot {{c}^{4}}\\left( \\text{NO} \\right)\\cdot c\\left( {{\\text{O}}_{2}} \\right)}$
","其他条件不变时,增大$\\dfrac{n\\left( {{\\text{O}}_{2}} \\right)}{n\\left( \\text{NO} \\right)}$,$\\text{NO}$的平衡转化率下降
","键角:$\\text{N}{{\\text{H}}_{3}}\\gt {{\\text{H}}_{2}}\\text{O}$
"]$\rm A$.使用催化剂可以降低反应的活化能,但不改变反应的焓变,$\rm A$错误;
$\rm B$.由反应方程式可知该反应的平衡常数为:$K=\dfrac{{{c}^{4}}\left( {{\text{N}}_{2}} \right)\cdot {{c}^{6}}\left( {{\text{H}}_{2}}\text{O} \right)}{{{c}^{4}}\left( \text{N}{{\text{H}}_{3}} \right)\cdot {{c}^{4}}\left( \text{NO} \right)\cdot c\left( {{\text{O}}_{2}} \right)}$,$\rm B$错误;
$\rm C$.增大$\dfrac{n\left( {{\text{O}}_{2}} \right)}{n\left( \text{NO} \right)}$的比值,相当于增大$c\left( {{\text{O}}_{2}} \right)$,平衡右移,则$\text{NO}$的平衡转化率增大,$\rm C$错误;
$\rm D$.在$\text{N}{{\text{H}}_{\text{3}}}$分子中仅含$\rm 1$对孤电子对,而${{\text{H}}_{2}}\text{O}$含有$\rm 2$对,孤电子对越多,对键角的斥力越大,键角越小,所以有键角:$\text{N}{{\text{H}}_{3}}\gt {{\text{H}}_{2}}\text{O}$,$\rm D$正确;
故选:$\rm D$
高中 | 化学平衡常数题目答案及解析(完整版)
