高中 | 杂化轨道理论 题目答案及解析
稿件来源:高途
高中 | 杂化轨道理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
杂化轨道理论
化合物$\rm A$是一种常见的食品添加剂,被广泛应用于酱油等调味品中,$\rm A$的结构如图所示。其中$\rm X$、$\rm Y$、$\rm Z$、$\rm Q$、$\rm W$为原子序数依次增大的短周期主族元素,$\rm Q$的原子最外层电子数是电子层数的$\rm 3$倍。下列说法正确的是$(\quad\ \ \ \ )$
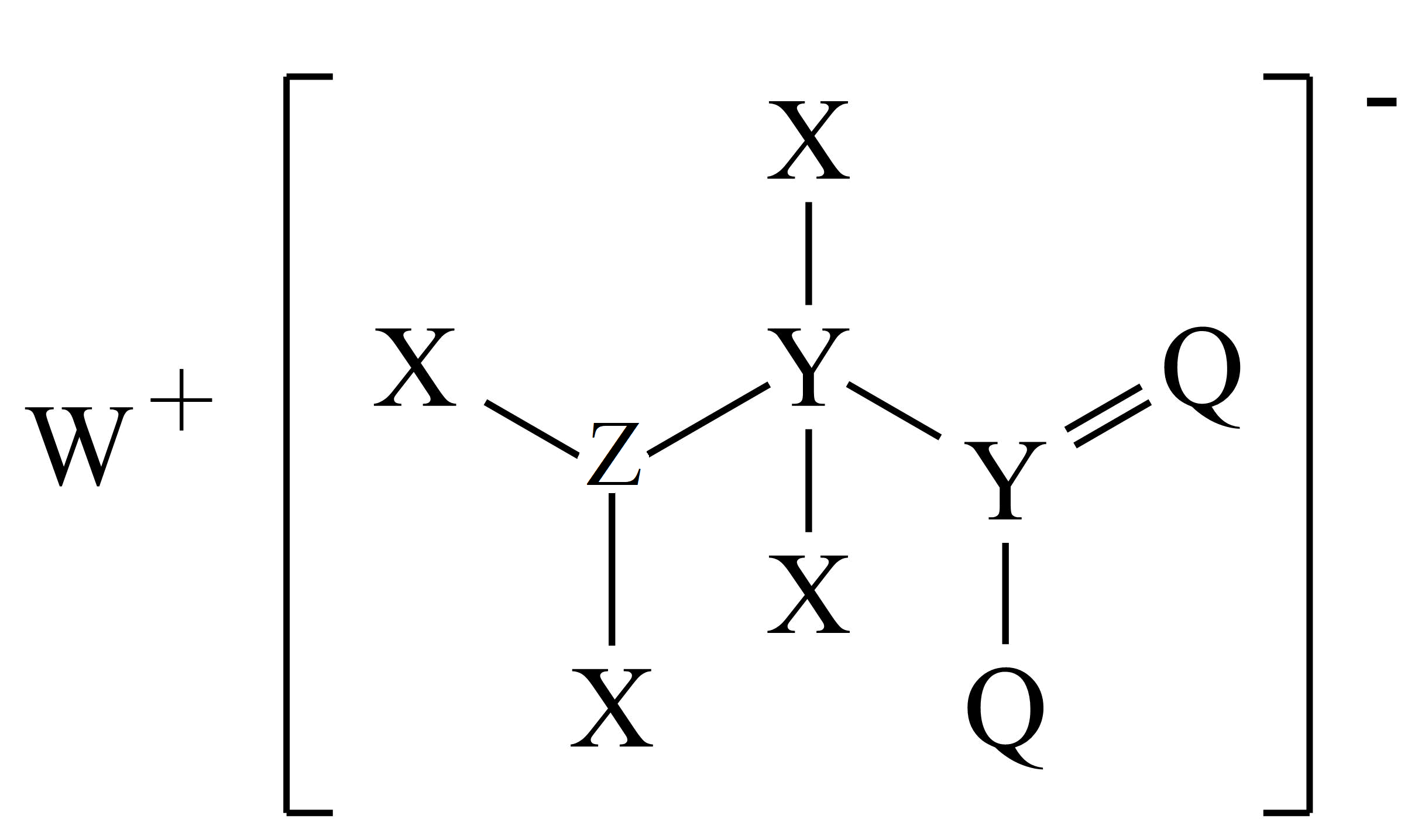
$\\rm YQ_{2}$与$\\rm ZQ_{2}$的空间构型均为直线型
","$\\rm W$单质的熔点大于$\\rm Y$单质
","$\\rm Y$、$\\rm Z$、$\\rm Q$原子的杂化方式均为$\\rm sp^{3}$
","最高价氧化物对应的水化物的酸性$\\rm Z\\gt Y$
"]其中$\rm X$、$\rm Y$、$\rm Z$、$\rm Q$、$\rm W$为原子序数依次增大的短周期主族元素,$\rm Q$的原子最外层电子数是电子层数的$\rm 3$倍,$\rm Q$为$\rm O$元素,由结构图可知:$\rm X$、$\rm Y$、$\rm Z$所成共价键的键数目分别为$\rm 1$、$\rm 4$、$\rm 3$、$\rm 2$,则它们分别为$\rm H$、$\rm C$、$\rm N$,而$\rm W$能形成稳定的一价阳离子,则其为$\rm Na$。
$\rm A$.$\rm CO_{2}$的空间构型为直线型,$\rm NO_{2}$中心原子价层电子对数为$\rm 2+$ $\dfrac{\text{1}}{\text{2}}\left( \text{5-2}\times \text{2} \right)\rm =3$,空间构型为$\rm V$型,故$\rm A$错误;
$\rm B$.$\rm C$单质的熔点高于$\rm Na$,故$\rm B$错误;
$\rm C$.由结构式可知,$\rm C$、$\rm N$的价层电子对数都是$\rm 4$,杂化方式均$\rm sp^{3}$,$\rm O$的价层电子对数是$\rm 3$,为$\rm sp^{2}$杂化,故$\rm C$错误;
$\rm D$.非金属性:$\rm N\gt C$,非金属性越强,元素最高价氧化物对应的水化物的酸性越强,则酸性:$\rm HNO_{3}\gt H_{2}CO_{3}$,故$\rm D$正确;
故选:$\rm D$
高中 | 杂化轨道理论题目答案及解析(完整版)
