高中 | 配合物理论 题目答案及解析
稿件来源:高途
高中 | 配合物理论题目答案及解析如下,仅供参考!
选修三
第二章 分子结构与性质
第二节 分子的立体结构
配合物理论
配合物二草酸合铜$\rm \left( Ⅱ\right)$酸钾$\rm {{\text{K}}_{2}}\left[ \text{Cu}{{\left( {{\text{C}}_{2}}{{\text{O}}_{4}} \right)}_{2}} \right](\textit{M}=318\;\text{g}/\text{mol})$,是制备金属有机框架材料的一种前驱体。某研究小组开展探究实验,步骤如下:
步骤$\rm I$:$\rm 80\; ^\circ \text{C}$下,$\rm \text{100\;\rm mL}$水中依次加入$\rm 0.024\;\rm \text{mol}\;{{\text{H}}_{2}}{{\text{C}}_{2}}{{\text{O}}_{4}}\cdot 2{{\text{H}}_{2}}\text{O}、0.016\;\rm \text{mol}\;{{\text{K}}_{2}}\text{C}{{\text{O}}_{3}}$充分反应后,得到混合溶液$\rm M$;
步骤Ⅱ:混合溶液$\rm M$中加入$\rm \text{0.008\;\rm mol\;\rm CuO}$充分反应,趁热过滤得滤液$\rm N$;
步骤Ⅲ: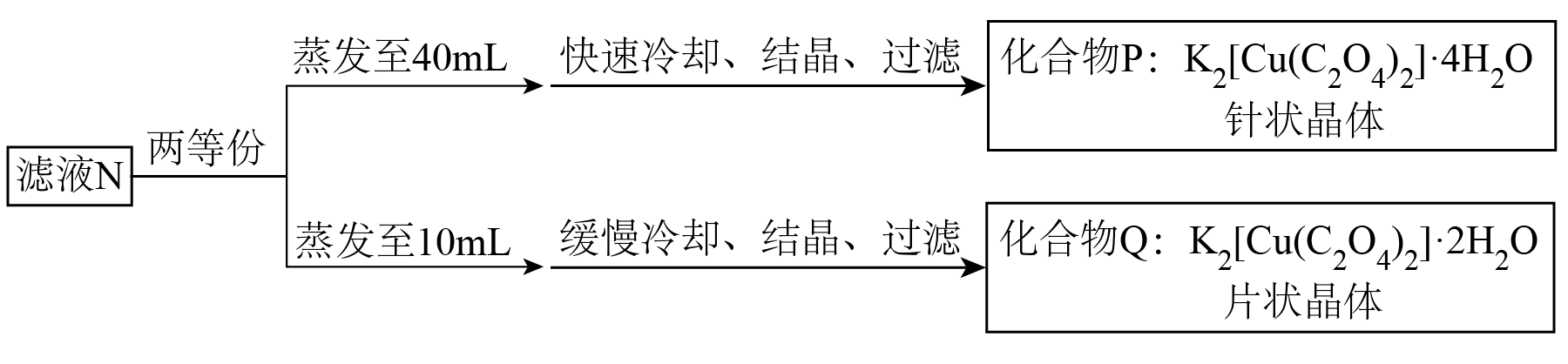
步骤Ⅳ:$\rm 200\;^\circ \text{C}$加热脱水,化合物$\rm P$、化合物$\rm Q$均转化为$\rm {{\text{K}}_{2}}\left[ \text{Cu}{{\left( {{\text{C}}_{2}}{{\text{O}}_{4}} \right)}_{2}} \right]$。
已知:
$\rm i$.$\rm 25\;^\circ \text{C}$时,$\rm {{\text{H}}_{2}}{{\text{C}}_{2}}{{\text{O}}_{4}}$的$\rm {\textit{K}_{\text{a}1}}=5.6\times {{10}^{-2}}、{\textit{K}_{a2}}=5.4\times {{10}^{-5}};{{\text{H}}_{2}}\text{C}{{\text{O}}_{3}}$的$\rm {\textit{K}_{\text{a}1}}=4.5\times {{10}^{-7}}、{\textit{K}_{{a\text{2}}}}=4.7\times {{10}^{-11}}$。
ⅱ.$\rm {{\text{K}}_{2}}\left[ \text{Cu}{{\left( {{\text{C}}_{2}}{{\text{O}}_{4}} \right)}_{2}} \right]$微溶于冷水、易溶于热水,在约$\rm 250\;^\circ \text{C}$时分解。
请回答:
$\rm {{\text{K}}_{2}}\left[ \text{Cu}{{\left( {{\text{C}}_{2}}{{\text{O}}_{4}} \right)}_{2}} \right]\cdot 4{{\text{H}}_{2}}\text{O}$中,与$\rm \text{C}{{\text{u}}^{2+}}$形成配位键的配位原子是 $\rm ($填元素符号$\rm )$。
$\\rm O$
"]]提供电中,端基的氧原子有孤电子对,可与具有空轨道的金属离子形成配位键,则$\rm {{\text{K}}_{2}}\left[ \text{Cu}{{\left( {{\text{C}}_{2}}{{\text{O}}_{4}} \right)}_{2}} \right]\cdot 4{{\text{H}}_{2}}\text{O}$中,与$\rm \text{C}{{\text{u}}^{2+}}$形成配位键的配位原子是$\rm O$。
步骤$\rm I$所得的混合溶液$\rm M$,在$\rm 25\;^\circ \text{C}$时其$\rm \text{pH}$最接近于$\rm (\quad\ \ \ \ )$。
$\\rm 2$
","$\\rm 3$
","$\\rm 4$
","$\\rm 5$
"]步骤$\rm I$中$\rm \text{100\;\rm mL}$水中依次加入$\rm 0.024\;\rm \text{mol}\;{{\text{H}}_{2}}{{\text{C}}_{2}}{{\text{O}}_{4}}\cdot 2{{\text{H}}_{2}}\text{O}、0.016\;\rm \text{mol}\;{{\text{K}}_{2}}\text{C}{{\text{O}}_{3}}$,由于$\rm \textit{K}_{a2}({{\text{H}}_{2}}{{\text{C}}_{2}}{{\text{O}}_{4}}\rm )\gt \textit{K}_{a1}({{\text{H}}_{2}}\text{C}{{\text{O}}_{3}}\rm )$,充分反应后生成$\rm KHC_{2}O_{4}$和$\rm K_{2}C_{2}O_{4}$,根据$\rm K$元素守恒和$\rm C$元素守恒可知,溶液$\rm M$中含有$\rm 0.016\;\rm mol\;\rm KHC_{2}O_{4}$、$\rm 0.008\;\rm mol\;\rm K_{2}C_{2}O_{4}$,在$\rm 25\;^\circ \text{C}$时溶液中$\rm\textit{c}(H^{+})=\dfrac{\textit{c}\left( \text{H}{{\text{C}}_{\text{2}}}\text{O}_{4}^{-} \right){{\textit{K}}_{\text{a2}}}\left( {{\text{H}}_{\text{2}}}{{\text{C}}_{\text{2}}}{{\text{O}}_{\text{4}}} \right)}{\textit{c}\left( {{\text{C}}_{\text{2}}}\text{O}_{\text{4}}^{\text{2-}} \right)}\rm =\dfrac{\text{0}\text{.16}\times 5.4\times {{10}^{-5}}}{\text{0}\text{.08}}\;\text{mol/L=1}\text{.08}\times \text{1}{{\text{0}}^{\text{-4}}}\;\text{mol/L}$,则$\rm pH=-lg\text{1}\text{.08}\times \text{1}{{\text{0}}^{\text{-4}}}\rm ≈4$,
故选:$\rm C$
步骤Ⅱ,过滤去除杂质需趁热进行的原因是 。
防止遇冷后产物析出而损失
"]]$\rm {{\text{K}}_{2}}\left[ \text{Cu}{{\left( {{\text{C}}_{2}}{{\text{O}}_{4}} \right)}_{2}} \right]$微溶于冷水、易溶于热水,步骤Ⅱ,过滤去除杂质需趁热进行的原因是:防止遇冷后产物析出而损失。
下列说法不正确的是$\rm (\quad\ \ \ \ )$。
步骤$\\rm I$,制备混合溶液$\\rm M$时,$\\rm {{\\text{K}}_{2}}\\text{C}{{\\text{O}}_{3}}$应一次性快速加入,以确保反应完全
","步骤Ⅳ,应用水浴控制温度,以避免$\\rm {{\\text{K}}_{2}}\\left[ \\text{Cu}{{\\left( {{\\text{C}}_{2}}{{\\text{O}}_{4}} \\right)}_{2}} \\right]$分解
","热重分析法测得$\\rm {{\\text{K}}_{2}}\\left[ \\text{Cu}{{\\left( {{\\text{C}}_{2}}{{\\text{O}}_{4}} \\right)}_{2}} \\right]\\cdot \\textit{x}{{\\text{H}}_{2}}\\text{O}$样品完全脱水后质量降低$\\rm 10.17\\%$,则$\\rm \\textit{x}=4$
","粉末形态的化合物$\\rm P$和化合物$\\rm Q$,可通过$\\rm X$射线衍射法进行区分
"]$\rm A$.步骤$\rm I$,制备混合溶液$\rm M$时,$\rm {{\text{K}}_{2}}\text{C}{{\text{O}}_{3}}$应缓慢多次加入,使反应更加充分,确保反应完全,$\rm A$错误;
$\rm B$.$\rm {{\text{K}}_{2}}\left[ \text{Cu}{{\left( {{\text{C}}_{2}}{{\text{O}}_{4}} \right)}_{2}} \right]$在约$\rm 250\;^\circ \text{C}$时分解,步骤Ⅳ中$\rm 200\;^\circ \text{C}$加热脱水,沸水浴只能控制温度$\rm 100\;^\circ \rm C$,$\rm B$错误;
$\rm C$.热重分析法测得$\rm {{\text{K}}_{2}}\left[ \text{Cu}{{\left( {{\text{C}}_{2}}{{\text{O}}_{4}} \right)}_{2}} \right]\cdot \textit{x}{{\text{H}}_{2}}\text{O}$样品完全脱水后质量降低$\rm 10.17\%$,则$\rm H_{2}O$在$\rm {{\text{K}}_{2}}\left[ \text{Cu}{{\left( {{\text{C}}_{2}}{{\text{O}}_{4}} \right)}_{2}} \right]\cdot \textit{x}{{\text{H}}_{2}}\text{O}$中的质量分数为$\rm 10.17\%$,$\rm \dfrac{18\textit{x}}{18\textit{x}+318}=0.1017$,解得$\rm \textit{x}=2$,$\rm C$错误;
$\rm D$.射线衍射法是利用$\rm X$射线探测晶体或分子结构的分析方法,粉末形态的化合物$\rm P$和化合物$\rm Q$,可通过$\rm X$射线衍射法进行区分,$\rm D$正确;
故选:$\rm ABC$
室温下,化合物$\rm P$在空气中会转化为化合物$\rm Q$。下列选项中,通过计算能得到混合样品中化合物$\rm P$和化合物$\rm Q$物质的量分数的是$\rm (\quad\ \ \ \ )$。
样品质量、钾的物质的量
","钾的物质的量、铜的物质的量
","铜的物质的量、草酸根的物质的量
","草酸根的物质的量、水的物质的量
"]$\rm A$.若已知样品质量$\rm (\textit{m}\;g)$、钾的物质的量$\rm (\textit{n}\;mol)$,可以设$\rm P$的物质的量为$\rm \textit{x}\;mol$,$\rm Q$的物质的量为$\rm \textit{y}\;mol$,$\rm 2 \textit{x}+2 \textit{y}=n$、$\rm 390 \textit{x}+351 \textit{y}= \textit{m}$,可以计算出$\rm \textit{x}$和$ y$的数值,可以得到混合样品中化合物$\rm P$和化合物$\rm Q$物质的量分数,$\rm A$选;
$\rm B$.若已知钾的物质的量$\rm ( \textit{a}\;mol)$、铜的物质的量$\rm ( \textit{b}\;mol)$,可以设$\rm P$的物质的量为$\rm \textit{x}\;mol$,$\rm Q$的物质的量为$\rm \textit{y}\;mol$,$\rm 2 \textit{x}+2 \textit{y}= \textit{a}$、$\rm \textit{x}+ \textit{y}=\textit{b}$,由于$\rm \textit{a}=2\textit{b}$,无法计算出$x$和$ y$的数值,无法得到混合样品中化合物$\rm P$和化合物$\rm Q$物质的量分数,$\rm B$不选;
$\rm C$.若已知铜的物质的量$\rm (\textit{a}\;mol)$、草酸根的物质的量$\rm (\textit{b}\;mol)$,可以设$\rm P$的物质的量为$\rm\textit{x}\;mol$,$\rm Q$的物质的量为$\rm \textit{y}\;mol$,$x+y=a$、$\rm 2 \textit{x}+2 \textit{y}= \textit{b}$,由于$ 2a=b$,无法计算出$ x$和$ y$的数值,无法得到混合样品中化合物$\rm P$和化合物$\rm Q$物质的量分数,$\rm C$不选;
$\rm D$.若已知草酸根的物质的量$\rm (\textit{a}\;mol)$、水的物质的量$\rm (\textit{b}\;mol)$,可以设$\rm P$的物质的量为$\rm \textit{x}\;mol$,$\rm Q$的物质的量为$\rm \textit{y}\;mol$,$ 2x+2y=a$、$4x+2y=b$,可以计算出$ x$和$ y$的数值,可以得到混合样品中化合物$\rm P$和化合物$\rm Q$物质的量分数,$\rm D$选;
故选:$\rm AD$
有同学认为:根据现有探究实验结果可知,化合物$\rm P$、化合物$\rm Q$结晶形状不同是由降温速率不同引起的。请判断该同学观点正误,并说明理由 。
错误,降温速率与浓度同时在变化,无法判断
"]]步骤Ⅲ中除了降温速率不同外,蒸发后溶液的体积也不同即浓度也不同,不能得出化合物$\rm P$、化合物$\rm Q$结晶形状不同是由降温速率不同引起的这样的观点。
高中 | 配合物理论题目答案及解析(完整版)
