高中 | 化学平衡常数 题目答案及解析
稿件来源:高途
高中 | 化学平衡常数题目答案及解析如下,仅供参考!
选修四
第二章 化学反应速率和化学平衡
第三节 化学平衡
化学平衡常数
$\text{C}{{\text{H}}_{4}}$可以将$\text{N}{{\text{O}}_{2}}$还原为${{\text{N}}_{2}}$,反应原理为:$\text{C}{{\text{H}}_{4}}\left( \text{g} \right)+2\text{N}{{\text{O}}_{2}}\left( \text{g} \right)\rightleftharpoons \text{C}{{\text{O}}_{2}}\left( \text{g} \right)+{{\text{N}}_{2}}\left( \text{g} \right)+2{{\text{H}}_{2}}\text{O}\left( \text{l} \right)\qquad\Delta { H}\lt 0$,$\text{N}{{\text{O}}_{2}}\left( \text{g} \right)$的平衡转化率随温度或压强的变化如图所示。下列说法错误的是$(\qquad)$
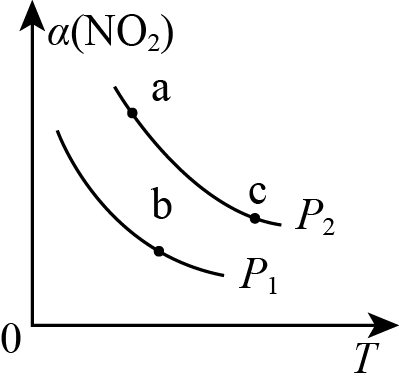
压强:${{{P}}_{1}}\\lt {{{P}}_{2}}$
","反应速率:${v}\\left( \\rm {a} \\right)\\lt {v}\\left(\\rm {c} \\right)$
","平衡常数:${{{K}}_{\\rm {a}}}\\gt {{{K}}_{\\rm {b}}}\\gt {{{K}}_{\\rm {c}}}$
","气体的颜色:$\\rm \\operatorname{a}$深,$\\rm {c}$浅
"]$\rm A$.该反应正反应气体分子数减小,同温时增大压强,$\text{N}{{\text{O}}_{2}}$平衡转化率增大,压强:${{ {P}}_{1}}\lt {{ {P}}_{2}}$,$\rm A$正确;
$\rm B$.由图可知$\rm a$、$\rm c$两点, $\rm c$点$\rm NO_{2}$的平衡转化率更低、反应物浓度更大,且$\rm c$点温度更高,所以反应速率:$ {v}\left( \text{a} \right)\lt {v}\left( \text{c} \right)$,$\rm B$正确;
$\rm C$.根据图示,升高温度,$\rm \text{N}{{\text{O}}_{2}}$平衡转化率减小,该反应放热,温度升高,平衡常数减小,温度:$\rm a\lt b\lt c$,平衡常数:${{ {K}}_{\text{a}}}\gt {{ {K}}_{\text{b}}}\gt {{ {K}}_{\text{c}}}$,$\rm C$正确;
$\rm D$.由图可知$\rm a$、$\rm c$两点压强均为$P_{2}$, $\rm c$点$\rm NO_{2}$的平衡转化率更低、$\rm NO_{2}$浓度更大,气体的颜色:$\rm \operatorname{a}$浅,$\rm \text{c}$深,$\rm D$错误。
故选:$\rm D$
高中 | 化学平衡常数题目答案及解析(完整版)
