高中 | 原电池工作原理 题目答案及解析
稿件来源:高途
高中 | 原电池工作原理题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第一节 原电池
原电池工作原理
$\rm LED$产品的使用为城市增添色彩。下图是氢氧燃料电池驱动$\rm LED$发光的一种装置示意图。下列叙述错误的是$(\qquad)$
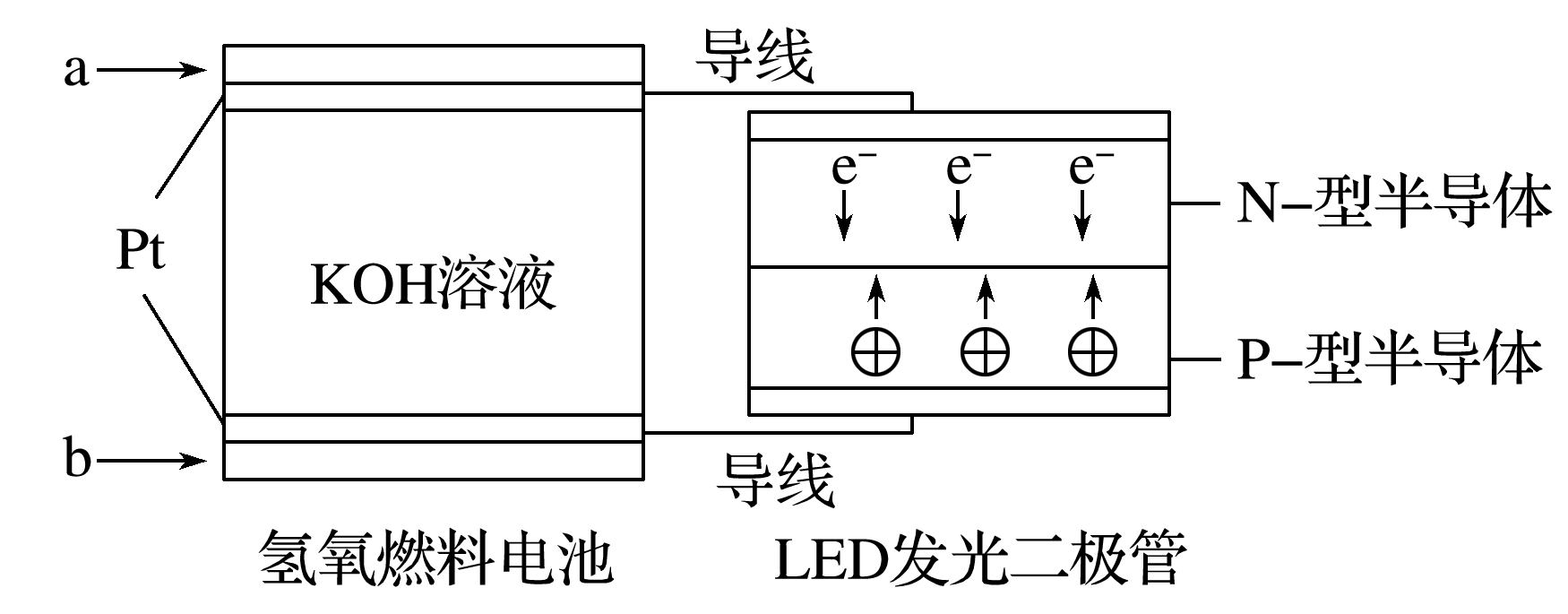
电极$\\rm a$发生反应:$\\rm \\mathrm{H}_{2}-2 \\mathrm{e}^{-}+2 \\mathrm{OH}^{-}=2 \\mathrm{H}_{2} \\mathrm{O}$
","电池放电后,电解质溶液中$\\rm \\text{O}{{\\text{H}}^{-}}$的物质的量基本不变
","电极$\\rm b$处应通入氧气,燃料电池实现了化学能到电能的转化
","电路中的电子从负极经外电路移向正极,再经过$\\rm KOH$溶液回到负极,形成闭合回路
"]氢氧燃料电池中,通入燃料氢气的电极是负极、通入氧气的电极是正极,电解质溶液呈碱性,则负极上电极反应式为$\rm {{\text{H}}_{2}}-2{{\text{e}}^{-}}+2O{{H}^{-}}=2{{\text{H}}_{2}}\text{O}$,正极电极反应式为$\rm {{\text{O}}_{2}}+2{{\text{H}}_{2}}\text{O}+4{{\text{e}}^{-}}=4O{{H}^{-}}$,总反应为:$\rm {{\text{O}}_{\text{2}}}\text{+2}{{\text{H}}_{\text{2}}}\text{=2}{{\text{H}}_{\text{2}}}\text{O}$。根据$\rm LED$发光二极管中电子移动方向可知,$\rm b$是原电池正极、$\rm a$是负极,原电池工作时,电子从负极经外电路到正极,溶液中阴离子移向负极,阳离子移向正极,据此分析解答。
$\rm A$.据分析可知,电极$\rm a$是负极,电极反应为:$\rm {{\text{H}}_{2}}-2{{\text{e}}^{-}}+2O{{H}^{-}}=2{{\text{H}}_{2}}\text{O}$,$\rm A$正确;
$\rm B$.电池总反应为:$\rm {{\text{O}}_{\text{2}}}\text{+2}{{\text{H}}_{\text{2}}}\text{=2}{{\text{H}}_{\text{2}}}\text{O}$,不消耗$\rm \text{O}{{\text{H}}^{-}}$,电池放电后,电解质溶液中$\rm \text{O}{{\text{H}}^{-}}$的物质的量基本不变,$\rm B$正确;
$\rm C$.据分析可知,电极$\rm b$为正极,通入氧气,该装置将化学能转化为电能最终转化为光能,$\rm C$正确;
$\rm D$.电路中的电子从负极经外电路到正极,但是电子不经过$\rm KOH$溶液,$\rm D$错误。
故选:$\rm D$
高中 | 原电池工作原理题目答案及解析(完整版)
