高中 | 氧化还原反应方程式的书写及配平 题目答案及解析
稿件来源:高途
高中 | 氧化还原反应方程式的书写及配平题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第三节 氧化还原反应
氧化还原反应方程式的书写及配平
某工厂采用如下工艺处理镍钴矿硫酸浸取液$\rm ($含$\text{N}{{\text{i}}^{2+}}$、$\text{C}{{\text{o}}^{2+}}$、$\text{M}{{\text{g}}^{2+}}$、$\text{F}{{\text{e}}^{2+}}$、$\text{F}{{\text{e}}^{3+}}$、$\text{M}{{\text{n}}^{2+}}\rm )$实现镍、钴、镁元素的回收。

已知:$\rm 1.$过一硫酸$\rm ({{\text{H}}_{2}}\text{S}{{\text{O}}_{5}}\rm )$的电离第一步完全,第二步微弱。
$\rm 25$ $\rm ^\circ\rm C$时,相关物质的${{K}_{\text{sp}}}$如下:
| 物质 | $\text{Fe}{{\left( \text{OH} \right)}_{3}}$ | $\text{Co}{{\left( \text{OH} \right)}_{2}}$ | $\text{Ni}{{\left( \text{OH} \right)}_{2}}$ | $\text{Mg}{{\left( \text{OH} \right)}_{2}}$ |
| ${{K}_{\text{sp}}}$ | ${{10}^{-38}}$ | ${{10}^{-14.7}}$ | $a$ | $b$ |
回答下列问题:
$\rm Ni$属于元素周期表的 区。
$\\rm d$
"]]镍元素的原子序数为$\rm 28$,基态原子的价电子排布式为$\rm 3d^{8}4s^{2}$,位于元素周期表的$\rm d$区;
混合气在“氧化”中,产生${{\text{H}}_{2}}\text{S}{{\text{O}}_{5}}$,其中$\rm S$的化合价为 。
$\\rm +6$
"]]过一硫酸可以看做过氧化氢中的一个氢原子被磺酸基取代,分子的结构式为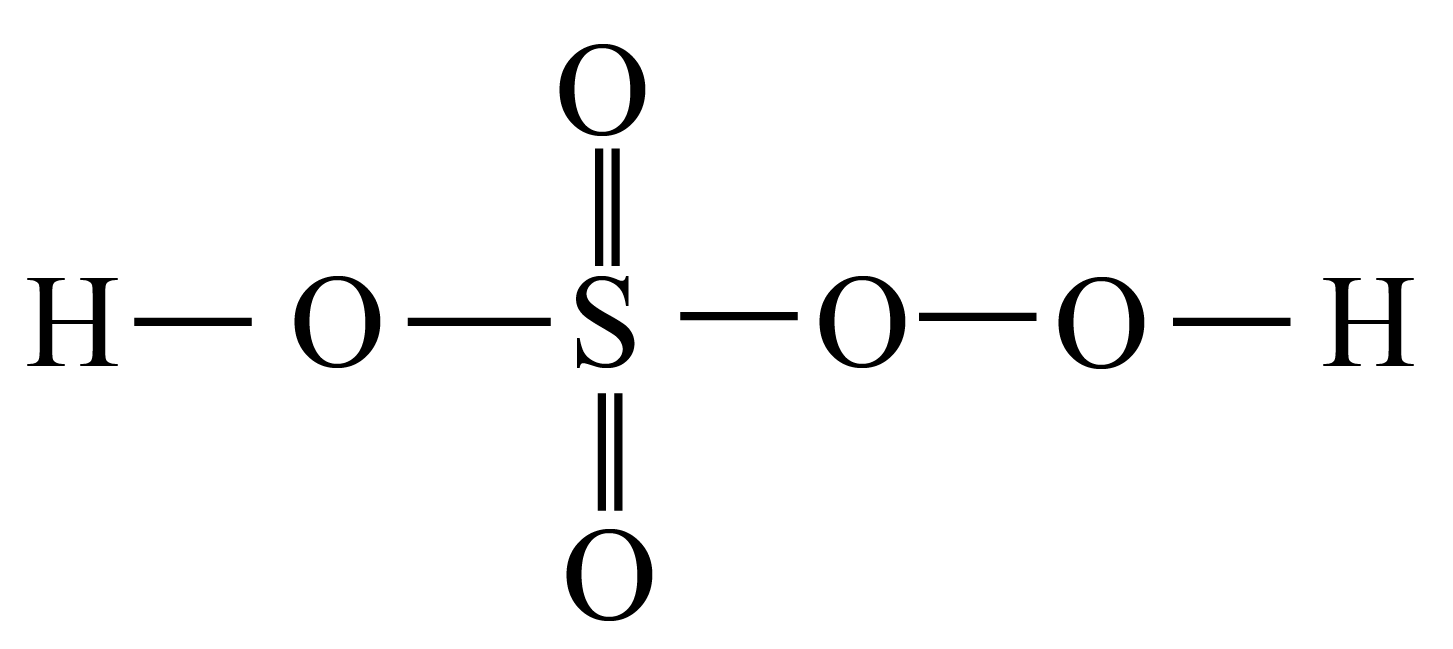 ,由结构式可知,分子中硫元素形成$\rm 6$个共价键,化合价为$\rm +6$价;
,由结构式可知,分子中硫元素形成$\rm 6$个共价键,化合价为$\rm +6$价;
“滤渣”的成分之一是软锰矿的主要成分,由${{\text{H}}_{2}}\text{S}{{\text{O}}_{5}}$氧化产生,该反应的离子方程式为 ;其可用于实验室制取氯气,该反应的离子方程式为 。
$\\rm Mn^{2+}+HSO_{5}^{-}\\rm +H_{2}O= MnO_{2}↓+SO_{\\text{4}}^{\\text{2-}}\\rm +3H^{+}$ ; $\\text{Mn}{{\\text{O}}_{\\text{2}}}\\text{+4}{{\\text{H}}^{+}}\\text{+2C}{{\\text{l}}^{-}}\\begin{matrix} \\underline{\\underline{_{\\triangle }}} \\\\ {} \\\\\\end{matrix}\\text{M}{{\\text{n}}^{\\text{2+}}}\\text{+C}{{\\text{l}}_{\\text{2}}}\\uparrow \\text{+2}{{\\text{H}}_{\\text{2}}}\\text{O}$
"]]由题意可知,生成二氧化锰的反应为溶液中的锰离子与过一硫酸溶液反应生成二氧化锰沉淀、硫酸根离子和氢离子,反应的离子方程式为$\rm Mn^{2+}+HSO_{5}^{-}\rm +H_{2}O= MnO_{2}↓+SO_{\text{4}}^{\text{2-}}\rm +3H^{+}$;二氧化锰制备氯气的反应为二氧化锰与浓盐酸共热反应生成氯化锰、氯气和水,反应的离子方程式为$\text{Mn}{{\text{O}}_{\text{2}}}\text{+4}{{\text{H}}^{+}}\text{+2C}{{\text{l}}^{-}}\begin{matrix} \underline{\underline{_{\triangle }}} \\ {} \\\end{matrix}\text{M}{{\text{n}}^{\text{2+}}}\text{+C}{{\text{l}}_{\text{2}}}\uparrow \text{+2}{{\text{H}}_{\text{2}}}\text{O}$;
若使$\text{F}{{\text{e}}^{3+}}$沉淀完全$\rm ($浓度$\le 1.0\times {{10}^{-5}}\rm )$,需调节$\rm pH$不低于 。
$\\rm 3$
"]]由溶度积可知,溶液中铁离子完全沉淀时,溶液中氢氧根离子浓度大于$\sqrt[3]{\dfrac{{{10}^{-38}}}{1.0\times {{10}^{-5}}\text{mol/L}}}={{10}^{-11}}\text{ mol/L}$,则溶液的$\rm pH$不低于$\rm 3$
上述表格中$a$ $ b($填“大于”、“小于”或“无法确定”$\rm )$。
小于
"]]由分析可知,加入氢氧化钠溶液时,溶液中镍离子优先产生沉淀,说明氢氧化镍的溶度积小于氢氧化镁;
“沉钴镍”后需将钴镍渣洗涤干净,实验室检验其是否洗净的方法是 。
取最后一次洗涤液少许于试管中,加入酸化的$\\rm BaCl_{2}$溶液,若没有白色沉淀生成,说明洗涤干净
"]]检验钴镍渣是否洗净实际上就是检验溶液中是否存在硫酸根离子,具体操作为取最后一次洗涤液少许于试管中,加入酸化的$\rm BaCl_{2}$溶液,若没有白色沉淀生成,说明洗涤干净;
滤液$\rm 2$中含有的金属阳离子是 。
$\\rm Na^{+}$、$\\rm Mg^{2+}$
"]]由分析可知,沉钴镍中加入氢氧化钠溶液的目的将溶液中的镍离子、亚钴离子转化为氢氧化镍、氢氧化亚钴沉淀,过滤得到钴镍渣和镁离子、钠离子的滤液$\rm 2$。
高中 | 氧化还原反应方程式的书写及配平题目答案及解析(完整版)
高中 | 氧化还原反应方程式的书写及配平 题目答案及解析
稿件来源:高途
高中 | 氧化还原反应方程式的书写及配平题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第三节 氧化还原反应
氧化还原反应方程式的书写及配平
1、某工厂采用如下工艺处理镍钴矿硫酸浸取液含
、
、
、
、
、
实现镍、钴、镁元素的回收。

已知:过一硫酸
的电离第一步完全,第二步微弱。
时,相关物质的
如下:
| 物质 | ||||
回答下列问题:
1.1、属于元素周期表的 区。
1.2、混合气在“氧化”中,产生,其中
的化合价为 。
1.3、“滤渣”的成分之一是软锰矿的主要成分,由氧化产生,该反应的离子方程式为 ;其可用于实验室制取氯气,该反应的离子方程式为 。
1.4、若使沉淀完全
浓度
,需调节
不低于 。
1.5、上述表格中
填“大于”、“小于”或“无法确定”
。
1.6、“沉钴镍”后需将钴镍渣洗涤干净,实验室检验其是否洗净的方法是 。
1.7、滤液中含有的金属阳离子是 。
高中 | 氧化还原反应方程式的书写及配平题目答案及解析(完整版)
免责声明:
① 凡本站注明“稿件来源:高途”的所有文字、图片和音视频稿件,版权均属本网所有,任何媒体、网站或个人未经本网协议授权不得转载、链接、转贴或以其他方式复制发表。已经本站协议授权的媒体、网站,在下载使用时必须注明“稿件来源:高途”,违者本站将依法追究责任。
② 本站注明稿件来源为网络的文/图等稿件均为转载稿,本站转载出于非商业性的教育和科研之目的,并不意味着赞同其观点或证实其内容的真实性。如转载稿涉及版权等问题,请作者在两周内速来电或来函联系。
我国宇航员在中国空间站利用化学反应制作出了漂亮的奥运五环。
用含有、和少量的铝灰制备,工艺流程如下部分操作和条件略:
某小组同学探究溶液与溶液的反应。
“价一类”二维图是学习元素及其化合物知识的重要模型和工具。下图是关于硫及其化合物的“价一类”二维图。
氨和硝酸是重要的化工原料。合成氨及氨氧化制硝酸的工艺流程如下。
二氧化氯具体以强氧化性,是一种比较安全的消毒剂。实验小组以氯气和亚氯酸钠为原料制备二氧化氯并探究其性质。




