高中 | 化学反应热的计算 题目答案及解析
稿件来源:高途
高中 | 化学反应热的计算题目答案及解析如下,仅供参考!
选修四
第一章 化学反应与能量
第三节 化学反应热的计算
化学反应热的计算
一定温度下反应$\rm {{H}_{2}}(g)+{{I}_{2}}(g)\rightleftharpoons 2HI(g)$的能量与反应过程的关系如图,下列说法不正确的是$\rm (\qquad)$
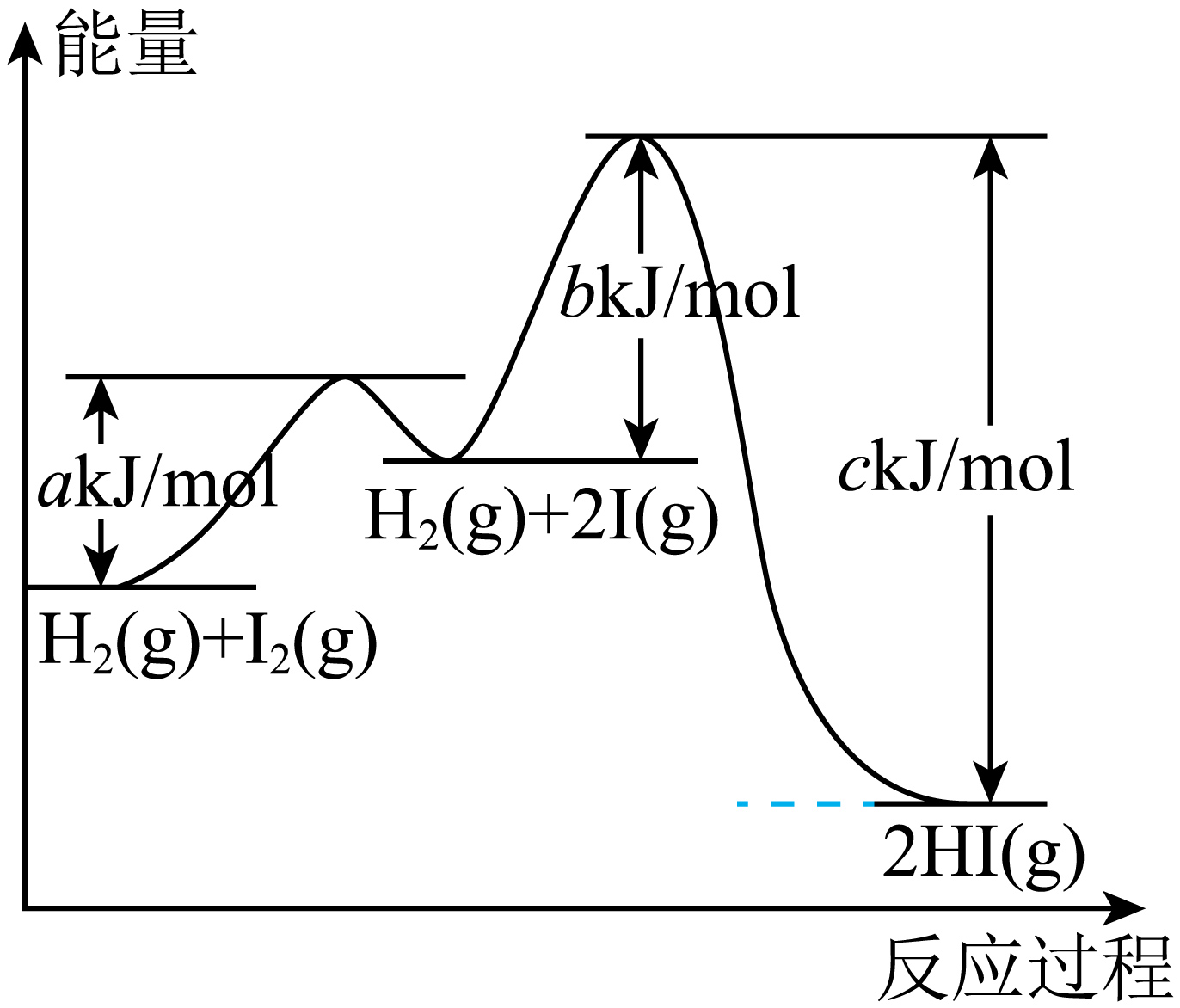
断开$\\rm I-I$键需要吸收能量
","$\\rm {{H}_{2}}(g)$和$\\rm {{I}_{2}}(g)$生成$\\rm 2HI(g)$的反应为放热反应
","该反应的$\\Delta H=-(c-b-a)\\ \\rm kJ\\cdot mo{{l}^{-1}}$
","$\\rm 1\\ mol\\ {{H}_{2}}(g)$和$\\rm 1\\ mol\\ {{I}_{2}}(g)$的总能量高于$\\rm 2\\ mol\\ HI(g)$的能量
"]$\rm A$.断裂旧键需要吸收能量,则断开$\rm I-I$键需要吸收能量,故$\rm A$正确。
$\rm B$.由图可知,$\rm 1\ mol$氢气和$\rm 1\ mol$碘蒸气的总能量高于$\rm 2\ mol$碘化氢的能量,则氢气和碘蒸气生成碘化氢的反应为放热反应,故$\rm B$正确。
$\rm C$.由图可知,反应$\rm {{H}_{2}}(g)+{{I}_{2}}(g)\rightleftharpoons 2HI(g)$分为两步进行,由于第一步的无法计算焓变,则总反应的焓变也无法得出,故$\rm C$错误。
$\rm D$.由图可知,$\rm 1\ mol$氢气和$\rm 1\ mol$碘蒸气的总能量高于$\rm 2\ mol$碘化氢的能量,故$\rm D$正确。
故选:$\rm C$
高中 | 化学反应热的计算题目答案及解析(完整版)
