高中 | 金属的电化学防护 题目答案及解析
稿件来源:高途
高中 | 金属的电化学防护题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第四节 金属的电化学腐蚀与防护
金属的电化学防护
国产航母山东舰采用模块制造,然后焊接组装而成。实验室模拟海水和淡水对焊接金属材料的影响,结果如图所示。下列分析正确的是 $(\quad\ \ \ \ )$
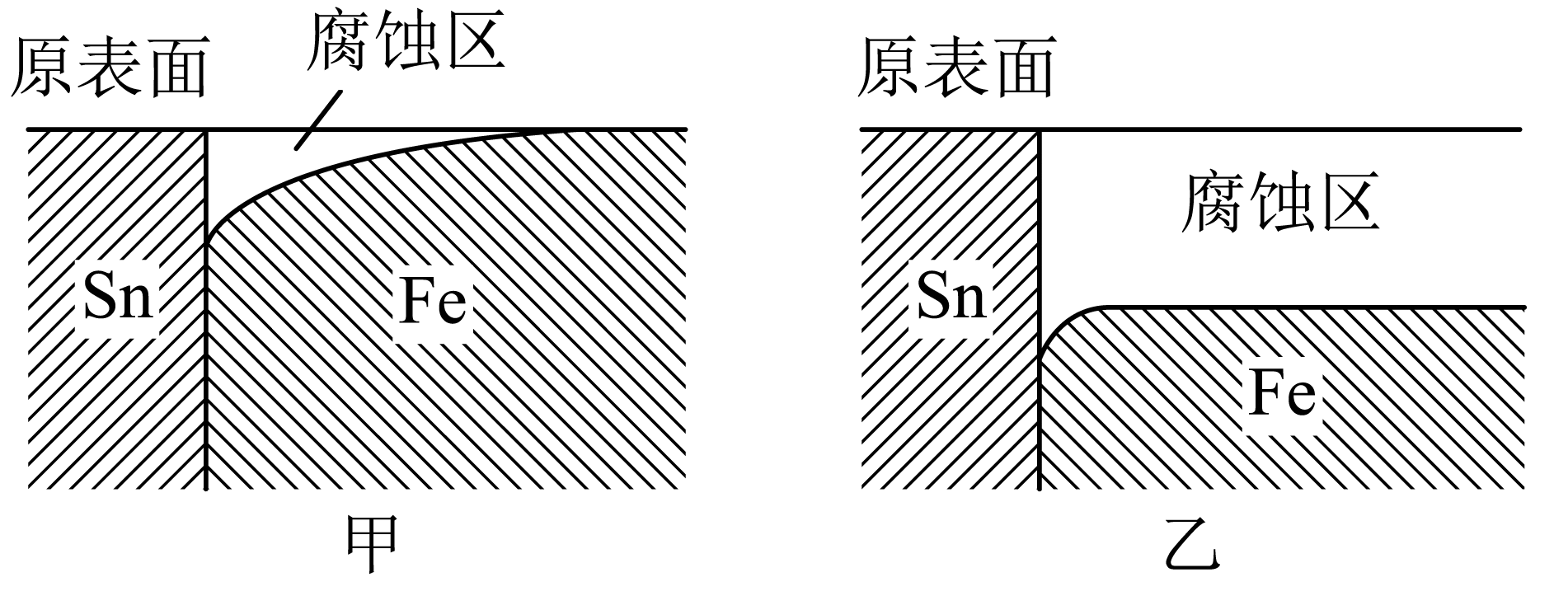
["
舰艇被腐蚀是因为形成了电解池
","甲是海水环境下的腐蚀情况
","被腐蚀时正极反应式为:$\\rm Fe-2e→Fe^{2+}$
","焊点附近用锌块打“补丁”延缓腐蚀
"][["D"]]
铁比锡活泼,在海水和淡水环境下,均是$\text{Fe}$为负极,$\text{Sn}$为正极,以此解题。
$\rm A$.由图可知,舰艇腐蚀是形成原电池,加快反应速率,$\rm A$错误;
$\rm B$.海水环境下电解质浓度较大,腐蚀更严重,乙是在海水环境下的腐蚀情况,$\rm B$错误;
$\rm C$.两种环境下,正极反应式为${{\text{O}}_{2}}+4{{\text{e}}^{-}}+2{{\text{H}}_{2}}\text{O}=4\text{O}{{\text{H}}^{-}}$,$\rm C$错误;
$\rm D$.锌可以和铁形成原电池,但是此时锌为负极,保护了舰体不被腐蚀,$\rm D$正确;
故选:$\rm D$
高中 | 金属的电化学防护题目答案及解析(完整版)
去刷题
今日推荐 ![]()
![]()
![]()
