高中 | 原电池工作原理 题目答案及解析
稿件来源:高途
高中 | 原电池工作原理题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第一节 原电池
原电池工作原理
近日,海南大学某团队以$\rm MXene$作为负极,$\rm AgCl/CuCl/FeOCl$作为正极,首次报道了一种基于天然海水电解液的可充电氯离子电池。
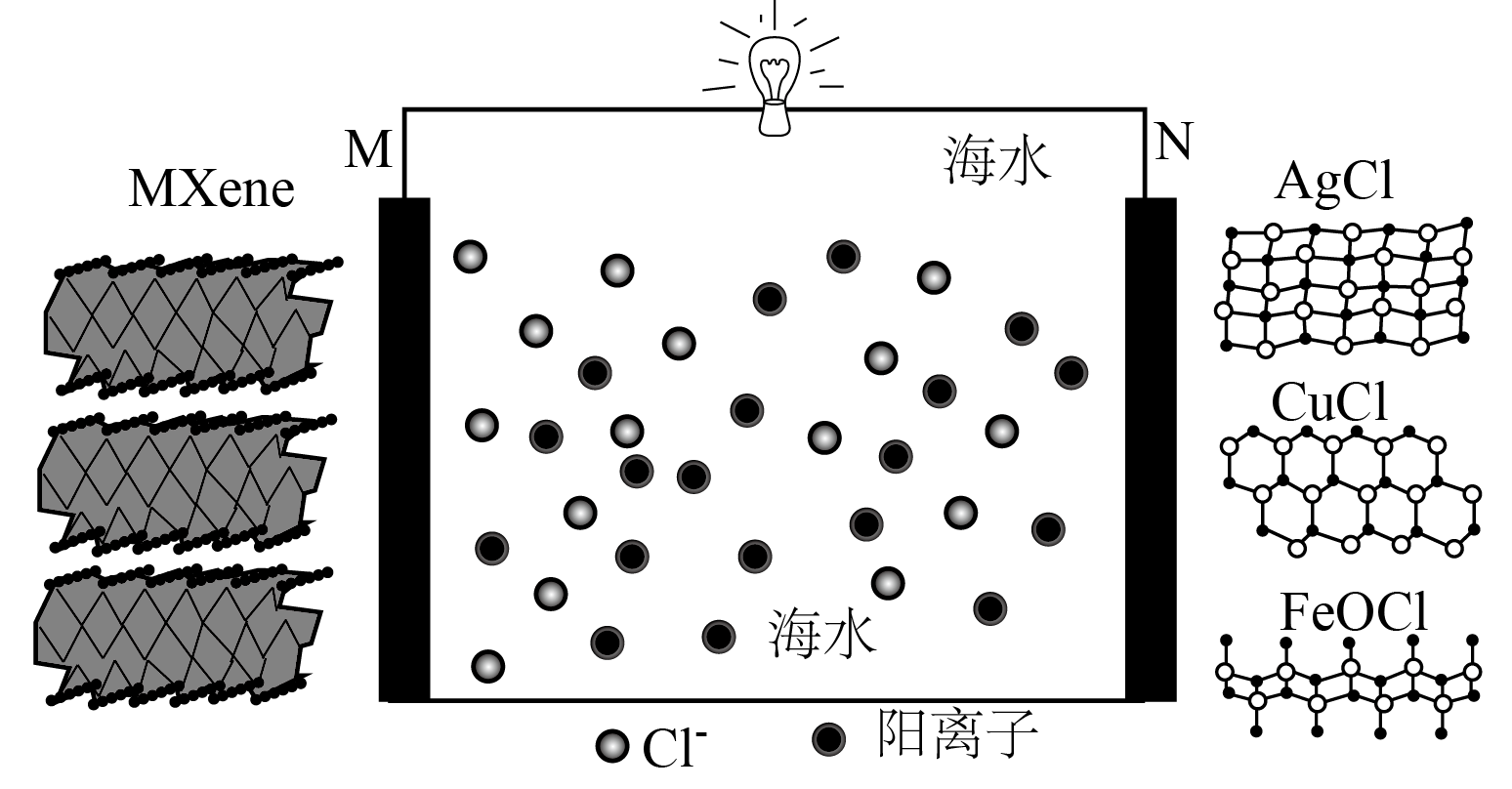
下列叙述错误的是$\rm (\qquad)$
放电时,$\\rm N$极发生还原反应
","放电时,发生迁移的$\\rm C{{l}^{-}}$数与阳离子数相等
","充电时,$\\rm M$极与电池的负极连接
","充电时,$\\rm N$极固体质量增加
"]原电池中,负极失电子发生氧化反应,正极得电子发生还原反应,电解质溶液中阳离子移向正极、阴离子移向负极。电池充电时,原电池负极与外接电源负极相连、正极与外接电源正极相连。
$\rm A$.如图所示,$\rm N$极为正极,$\rm M$为负极,放电时正极发生还原反应,故$\rm A$正确;
$\rm B$.放电时,氯离子向$\rm M$极迁移,$\rm N{{a}^{+}}$、$\rm M{{g}^{2+}}$等金属阳离子向$\rm N$极迁移,因为离子所带电荷不相等,根据电荷守恒,相同时间内向两极迁移的氯离子、阳离子数不相等,故$\rm B$错误;
$\rm C$.放电时$\rm M$为负极,则充电时$\rm M$极为阴极,与电源负极连接,故$\rm C$正确;
$\rm D$.充电时,$\rm N$极为阳极,发生氧化反应,根据阳极材料可能生成多种物质,如$\rm AgCl$、$\rm CuCl$、$\rm FeOCl$,阳极反应式之一是$\rm Cu+C{{l}^{-}}-{{e}^{-}}=CuCl$,$\rm N$极固体质量增加,故$\rm D$正确;
故选:B
高中 | 原电池工作原理题目答案及解析(完整版)
