高中 | 原电池工作原理 题目答案及解析
稿件来源:高途
高中 | 原电池工作原理题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第一节 原电池
原电池工作原理
电催化合成酯是一种选择性较好的方法,电催化羧酸与酮反应成酯的反应原理如图所示。下列说法错误的是$(\quad\ \ \ \ )$
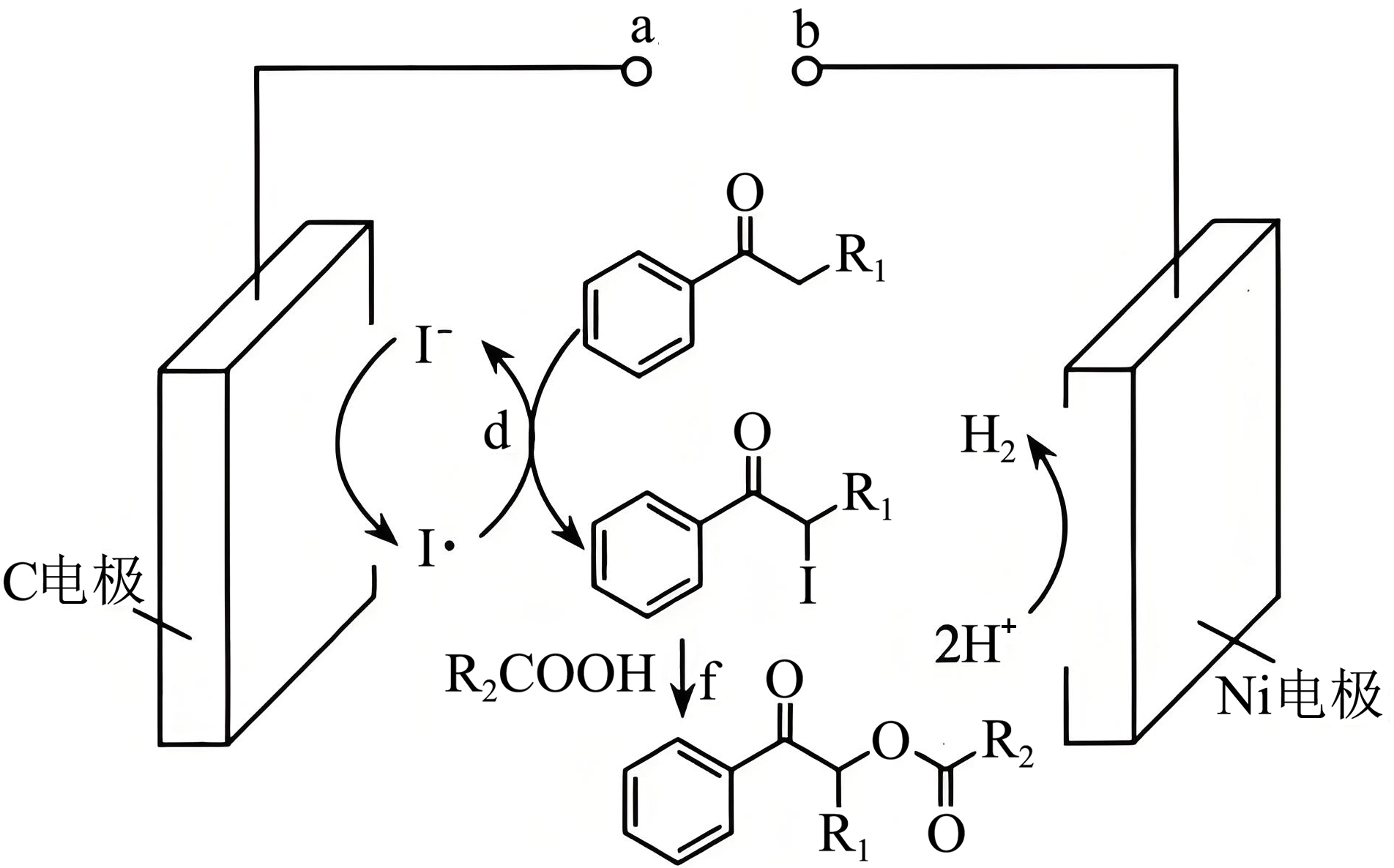
$\\rm b$为负极
","$\\rm C$电极的电极反应式为$\\rm I^{-}-e^{-}=I·$
","$\\rm I^{-}$是催化剂
","反应$\\rm d$还有一种产物是$\\rm H\\cdot $
"]由题干图示可知,$\rm Ni$电极由$\rm H^{+}$得到电子生成$\rm H_{2}$,发生还原反应,电极反应为:$\rm 2H^{+}+2e^{-}=H_{2}↑$,该电极为阴极,则$\rm b$为电源的负极,$\rm a$为电源的正极,$\rm C$电极为阳极,电极反应为:$\rm I^{-}-e^{-}=I·$,$\rm d$的反应为: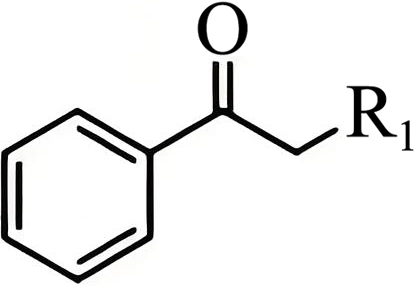 $\rm +\text{2I }\!\!\cdot\to $
$\rm +\text{2I }\!\!\cdot\to $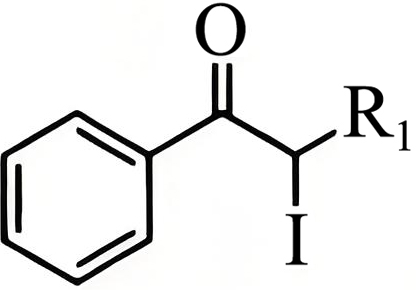 $\rm +H^{+}+I^{-}$,
$\rm +H^{+}+I^{-}$, $\rm +{{\text{R}}_{\text{2}}}\text{COOH}\to $
$\rm +{{\text{R}}_{\text{2}}}\text{COOH}\to $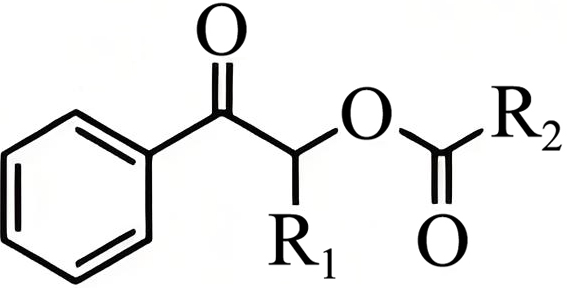 $\rm +HI$,据此分析解题。
$\rm +HI$,据此分析解题。
$\rm A$.由分析可知,$\rm b$为负极,$\rm A$正确;
$\rm B$.由分析可知,$\rm C$电极的电极反应式为$\rm I^{-}-e^{-}=I·$,$\rm B$正确;
$\rm C$.由分析可知,$\rm I^{-}$参与反应又重新生成,反应前后质量不变,故$\rm I^{-}$是催化剂,$\rm C$正确;
$\rm D$.由分析可知,反应$\rm d$还有一种产物是$\rm H^{+}$,$\rm D$错误;
故选:$\rm D$
高中 | 原电池工作原理题目答案及解析(完整版)
