高中 | 原电池工作原理 题目答案及解析
稿件来源:高途
高中 | 原电池工作原理题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第一节 原电池
原电池工作原理
新型水泥基电池具有成本低、环境友好和可充电性等优点,在绿色储能领域具有巨大的应用潜力。已知水泥基材料的孔结构充满了毛细孔水和游离水组成的孔溶液,孔溶液内的离子通过孔隙通道传输。该电池放电时原理如图所示,下列说法正确的是$(\qquad)$
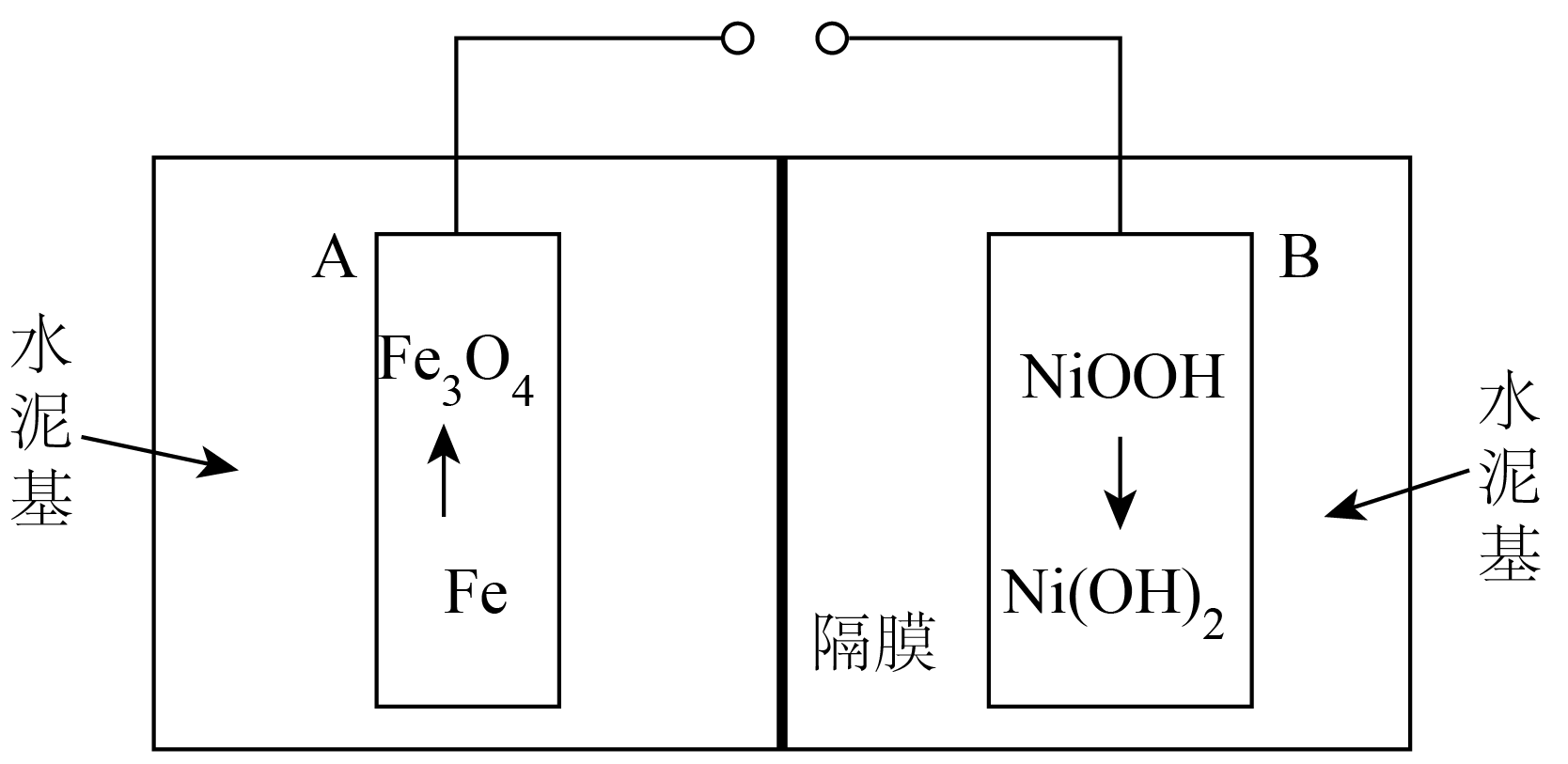
水泥基中孔溶液呈强酸性
","放电时,电极$\\rm B$发生氧化反应
","隔膜应为阳离子交换膜
","充电时,阳极的电极反应式为$\\text{Ni}{{\\left( \\text{OH} \\right)}_{2}}+\\text{O}{{\\text{H}}^{-}}-{{\\text{e}}^{-}}=\\text{NiOOH}+{{\\text{H}}_{2}}\\text{O}$
"]放电时,$\rm A$电极铁失电子生成四氧化三铁,$\rm A$是负极,负极反应式为$\rm 3Fe-8e^{-}+8OH^{-}=Fe_{3}O_{4}+4H_{2}O$;$\rm B$电极$\rm NiOOH$得电子生成$\rm Ni(OH)_{2}$,电极反应式为$\rm NiOOH+e^{-}+H_{2}O=Ni(OH)_{2}+OH^{-}$,$\rm B$是正极。
$\rm A\rm .$ $\rm Fe$、$\rm Fe_{3}O_{4}$、$\rm NiOOH$、$\rm Ni(OH)_{2}$均能与酸反应,水泥基中孔溶液不能呈强酸性,故$\rm A$错误;
$\rm B\rm .$ 放电时,电极$\rm B$镍元素化合价降低,发生还原反应,故$\rm B$错误;
$\rm C\rm .$ 根据电极反应式,负极消耗氢氧根离子、正极生成氢氧根离子,隔膜应为阴离子交换膜,故$\rm C$错误;
$\rm D\rm .$ 放电时,正极反应式为$\rm NiOOH+e^{-}+H_{2}O=Ni(OH)_{2}+OH^{-}$,充电时,阳极的电极反应式为$\text{Ni}{{\left( \text{OH} \right)}_{2}}+\text{O}{{\text{H}}^{-}}-{{\text{e}}^{-}}=\text{NiOOH}+{{\text{H}}_{2}}\text{O}$,故$\rm D$正确。
故选:$\rm D$
高中 | 原电池工作原理题目答案及解析(完整版)
