高中 | 原电池工作原理 题目答案及解析
稿件来源:高途
高中 | 原电池工作原理题目答案及解析如下,仅供参考!
选修四
第四章 电化学基础
第一节 原电池
原电池工作原理
一种新型的铅锂电池的充、放电示意图如图所示,下列说法错误的是$(\quad\ \ \ \ )$
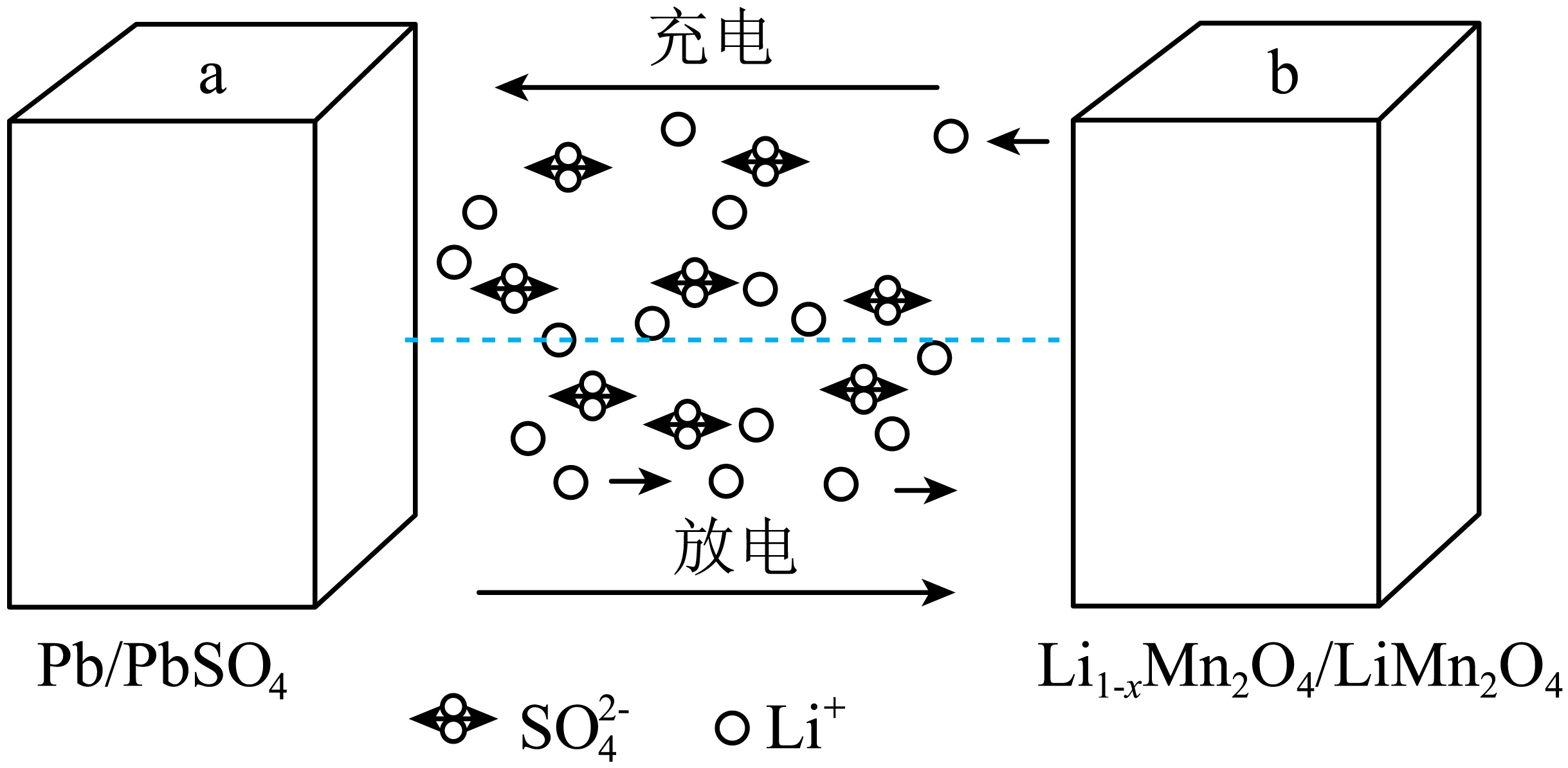
放电时,$\\text{SO}_{4}^{2-}$向电极$\\rm a$方向迁移
","充电时,$\\text{LiM}{{\\text{n}}_{2}}{{\\text{O}}_{4}}$中$\\rm Mn$元素被氧化
","放电时,正极反应式为$\\text{L}{{\\text{i}}_{1-x}}\\text{M}{{\\text{n}}_{2}}{{\\text{O}}_{4}}+x{{\\text{e}}^{-}}+x\\text{L}{{\\text{i}}^{+}}=\\text{LiM}{{\\text{n}}_{2}}{{\\text{O}}_{4}}$
","充电时,每转移$\\rm 1$ $\\rm mol$ ${{\\text{e}}^{-}}$,$\\rm a$极增重$\\rm 103.5$ $\\rm g$
"]由铅锂电池的充、放电示意图可知,电解质为$\text{L}{{\text{i}}_{2}}\text{S}{{\text{O}}_{4}}$溶液,放电时负极$\rm (a$极$\rm )$反应为$\mathrm{Pb}+\mathrm{SO}_{4}^{2-}-2 \mathrm{e}^{-}=\mathrm{PbSO}_{4}$,正极$\rm (b$极$\rm )$反应式为$\text{L}{{\text{i}}_{1-x}}\text{M}{{\text{n}}_{2}}{{\text{O}}_{4}}+x{{\text{e}}^{-}}+x\text{L}{{\text{i}}^{+}}=\text{LiM}{{\text{n}}_{2}}{{\text{O}}_{4}}$。
$\rm A$.放电时,阴离子向负极迁移,由分析知放电时$a$极为负极,$\text{SO}_{4}^{2-}$向电极$\rm a$方向迁移,故$\rm A$正确;
$\rm B$.充电时$\rm b$极为阳极, $\text{LiM}{{\text{n}}_{2}}{{\text{O}}_{4}}$转化为$\text{L}{{\text{i}}_{1-x}}\text{M}{{\text{n}}_{2}}{{\text{O}}_{4}}$,$\rm Mn$元素化合价升高,$\text{LiM}{{\text{n}}_{2}}{{\text{O}}_{4}}$中$\rm Mn$元素被氧化,故$\rm B$正确;
$\rm C$.有分析知放电时,$\rm b$极为正极,电极反应式为:$\text{L}{{\text{i}}_{1-x}}\text{M}{{\text{n}}_{2}}{{\text{O}}_{4}}+x{{\text{e}}^{-}}+x\text{L}{{\text{i}}^{+}}=\text{LiM}{{\text{n}}_{2}}{{\text{O}}_{4}}$,故$\rm C$正确;
$\rm D$.充电时$\rm a$极为阴极,电极反应式为$\text{PbS}{{\text{O}}_{4}}+2{{\text{e}}^{-}}=\text{Pb}+\text{SO}_{4}^{2-}$,生成的$\text{SO}_{4}^{2-}$进入电解质溶液中,外电路每转移$\rm 1$ $\rm mol$ ${{\text{e}}^{-}}$,$\rm a$极质量减轻$\rm 48$ $\rm g$,$\rm D$项错误;
故选:$\rm D$
高中 | 原电池工作原理题目答案及解析(完整版)
