高中 | 化学平衡常数 题目答案及解析
稿件来源:高途
高中 | 化学平衡常数题目答案及解析如下,仅供参考!
选修四
第二章 化学反应速率和化学平衡
第三节 化学平衡
化学平衡常数
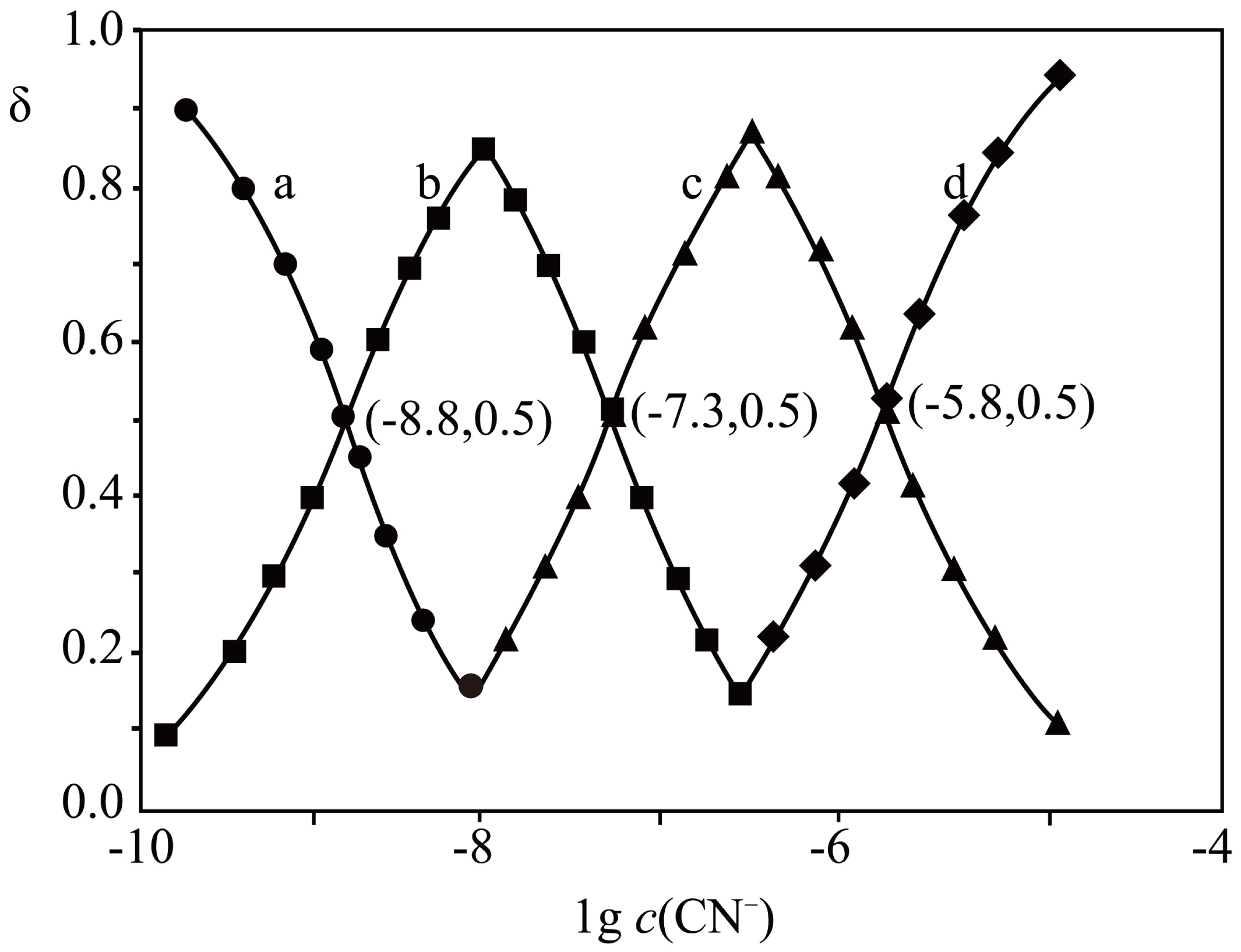
常温下,$\text{Z}{{\text{r}}^{4+}}$和$\text{C}{{\text{N}}^{-}}$形成${{\left[ \text{Zr}\left( \text{CN} \right) \right]}^{3+}}$、${{\left[ \text{Zr}{{\left( \text{CN} \right)}_{2}} \right]}^{2+}}$、${{\left[ \text{Zr}{{\left( \text{CN} \right)}_{3}} \right]}^{+}}$配离子,在$\text{Zr}{{\left( \text{N}{{\text{O}}_{3}} \right)}_{4}}$溶液加入$\text{KCN}$溶液,含$\text{Zr}$粒子分布系数$\delta $与$\lg c\left( \text{C}{{\text{N}}^{-}} \right)$关系如图所示。$(\qquad)$
已知:①$\delta\left( \text{Z}\text{r}^{4+}\right)=\dfrac{c\left( \text{Z}\text{r}^{4+}\right)}{c\left( \text{Z}\text{r}^{4+}\right)+c\left\{ \left[ \text{Zr}\left( \text{CN}\right)\right]^{3+}\right\}+c\left\{ \left[ \text{Zr}\left( \text{CN}\right)_{2}\right]^{2+}\right\}+c\left\{ \left[ \text{Zr}\left( \text{CN}\right)_{3}\right]^{+}\right\}}$;
②$\text{Z}\text{r}^{4+}+\text{C}\text{N}^{-}\rightleftharpoons\left[ \text{Zr}\left( \text{CN}\right)\right]^{3+}\qquad K_{1}$,$\text{Z}\text{r}^{4+}+2\text{C}\text{N}^{-}\rightleftharpoons\left[ \text{Zr}\left( \text{CN}\right)_{2}\right]^{2+}\qquad K_{2}$,$\text{Z}\text{r}^{4+}+3\text{C}\text{N}^{-}\rightleftharpoons\left[ \text{Zr}\left( \text{CN}\right)_{3}\right]^{+}\qquad K_{3}\left( K_{1}\lt K_{2}\lt K_{3}\right)$
下列叙述错误
$\\text{c}$曲线代表$\\delta \\left\\{ {{\\left[ \\text{Zr}{{\\left( \\text{CN} \\right)}_{2}} \\right]}^{2+}} \\right\\}$与$\\lg c\\left( \\text{C}{{\\text{N}}^{-}} \\right)$关系
","常温下,${{K}_{2}}={{10}^{7.3}}$
","$\\left[ \\text{Zr}\\left( \\text{CN}\\right)\\right]^{3+}+2\\text{C}\\text{N}^{-}\\rightleftharpoons\\left[ \\text{Zr}\\left( \\text{CN}\\right)_{3}\\right]^{+}\\qquad K=10^{13.1}$
","上述配离子中,${{\\left[ \\text{Zr}{{\\left( \\text{CN} \\right)}_{3}} \\right]}^{+}}$最稳定
"]根据络合方程式可知,随着$c\left( \text{C}{{\text{N}}^{-}} \right)$的增大,依次生成${{\left[ \text{Zr}\left( \text{CN} \right) \right]}^{3+}}$、${{\left[ \text{Zr}{{\left( \text{CN} \right)}_{2}} \right]}^{2+}}$、${{\left[ \text{Zr}{{\left( \text{CN} \right)}_{3}} \right]}^{+}}$,结合图像可知,$\rm a$,$\rm b$,$\rm c$,$\rm d$曲线依次代表$\text{Z}{{\text{r}}^{4+}}$,${{\left[ \text{Zr}\left( \text{CN} \right) \right]}^{3+}}$、${{\left[ \text{Zr}{{\left( \text{CN} \right)}_{2}} \right]}^{2+}}$、${{\left[ \text{Zr}{{\left( \text{CN} \right)}_{3}} \right]}^{+}}$与$\lg c\left( \text{C}{{\text{N}}^{-}} \right)$关系。由$\rm a$和$\rm b$曲线的交点($\rm -8.8$,$\rm 0.5$),可知$\text{Z}\text{r}^{4+}+\text{C}\text{N}^{-}\rightleftharpoons\left[ \text{Zr}\left( \text{CN}\right)\right]^{3+}\qquad K_{1}$,$K_{1}=\dfrac{\left[ \text{Zr}\left( \text{CN}\right)\right]^{3+}}{c\text{(Z}\text{r}^{\text{4+}})\times c\text{(C}\text{N}^{-})}=\dfrac{1}{10^{-8.8}}=10^{8.8}$。由$\rm b$和$\rm c$曲线的交点($\rm -7.3$,$\rm 0.5$)以及盖斯定律,可知$\left[ \text{Zr}\left( \text{CN}\right)\right]^{3+}+\text{C}\text{N}^{-}\rightleftharpoons\left[ \text{Zr}\left( \text{CN}\right)_{2}\right]^{2+}\qquad K_{\text{ii}}$, $K_{\text{ii}}=\dfrac{K_{\text{2}}}{K_{\text{1}}}=\dfrac{c\left\{ \left[ \text{Zr}\left( \text{CN}\right)_{2}\right]^{2+}\right\}}{c\left\{ \left[ \text{Zr}\left( \text{CN}\right)\right]^{3+}\right\}\times c(\rm CN^{-})}=\dfrac{1}{10^{-7.3}}=10^{7.3}$。由$\rm c$和$\rm d$曲线的交点($\rm -5.8$,$\rm 0.5$)以及盖斯定律,可知$\left[ \text{Zr}\left( \text{CN}\right)_{2}\right]^{2+}+\text{C}\text{N}^{-}\rightleftharpoons\left[ \text{Zr}\left( \text{CN}\right)_{3}\right]^{+}\qquad K_{\text{iii}}$,$K_{\text{iii}}=\dfrac{K_{\text{3}}}{K_{\text{2}}}=\dfrac{c\left\{ \left[ \text{Zr}\left( \text{CN}\right)_{3}\right]^{+}\right\}}{c\left\{ \left[ \text{Zr}\left( \text{CN}\right)_{2}\right]^{2+}\right\}\times c(\rm CN^{-})}=\dfrac{1}{10^{-5.8}}=10^{5.8}$,据此回答。
$\rm A$.由分析可知,$\text{c}$曲线代表$\delta \left\{ {\left\lbrack \mathrm{{Zr}}{\left( \mathrm{{CN}}\right) }_{2}\right\rbrack }^{2 + }\right\}$与$\lg c\left( \text{C}{{\text{N}}^{-}} \right)$关系,$\rm A$选项正确;
$\rm B$.由分析可知${{K}_{2}}={{10}^{7.3}}\times {{K}_{1}}={{10}^{7.3}}\times {{10}^{8.8}}={{10}^{16.1}}$,$\rm B$选项错误;
$\rm C$.根据盖斯定律可知,方程式$\rm ii$和$\rm iii$相加可得${{\left[ \text{Zr}\left( \text{CN} \right) \right]}^{3+}}+2\text{C}{{\text{N}}^{-}}\rightleftharpoons {{\left[ \text{Zr}{{\left( \text{CN} \right)}_{3}} \right]}^{+}}$,$K={{K}_{\text{ii}}}\times{{K}_{\text{iii}}}={{10}^{7.3}}\times {{10}^{5.8}}={{10}^{13.1}}$,$\rm C$选项正确;
$\rm D$.由分析可知${{K}_{3}}={{10}^{5.8}}\times {{K}_{2}}={{10}^{5.8}}\times {{10}^{16.1}}={{10}^{21.9}}$,因${{K}_{1}}={{10}^{8.8}},{{K}_{2}}={{10}^{16.1}},{{K}_{3}}={{10}^{21.9}}$,同一种阳离子与同一种配体形成配合物,平衡常数越大,对应配离子越稳定,因此${{\left[ \text{Zr}{{\left( \text{CN} \right)}_{3}} \right]}^{+}}$最稳定,$\rm D$选项正确;
故选:$\rm B$
高中 | 化学平衡常数题目答案及解析(完整版)
