高中 | 盐类水解常数 题目答案及解析
稿件来源:高途
高中 | 盐类水解常数题目答案及解析如下,仅供参考!
选修四
第三章 水溶液中的离子平衡
第三节 盐类的水解
盐类水解常数
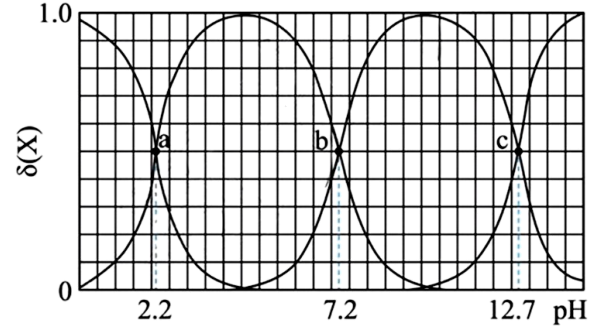
$298\text{ K}$时,在${{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}$溶液中滴入$\text{NaOH}$溶液,溶液中${{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}$、${{\text{H}}_{2}}\text{PO}_{4}^{-}$、$\text{HPO}_{4}^{2-}$、$\text{PO}_{4}^{3-}$的物质的量分数$\delta \left( \text{X} \right)$,$\delta \left( \text{X} \right)$随$\text{pH}$的变化如图所示,下列叙述错误的是$(\quad\ \ \ \ )$
${{K}_{\\text{a2}}}\\left( {{\\text{H}}_{\\text{3}}}\\text{P}{{\\text{O}}_{\\text{4}}} \\right)$的数量级为${{10}^{-8}}$
","${K}_{\\mathrm{h}}\\left( {{\\mathrm{H}}_{2}{\\mathrm{{PO}}}_{4}^{ - }}\\right)= {1.0} \\times{10}^{-{11.8}}$
","等体积、等浓度的$\\text{N}{{\\text{a}}_{2}}\\text{HP}{{\\text{O}}_{4}}$与$\\text{N}{{\\text{a}}_{3}}\\text{P}{{\\text{O}}_{4}}$溶液混合后,$c\\left( \\text{HPO}_{\\text{4}}^{\\text{2-}} \\right)\\lt c\\left( \\text{PO}_{\\text{4}}^{\\text{3-}} \\right)$
","$\\text{pH}=7$时,$c\\left( {{\\text{H}}_{\\text{2}}}\\text{PO}_{\\text{4}}^{-} \\right)\\gt c\\left( \\text{HPO}_{\\text{4}}^{\\text{2-}} \\right)$
"]分析:
由$\rm pH$变化可知,在${{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}$溶液中滴入$\text{NaOH}$溶液,溶液中${{\text{H}}_{3}}\text{P}{{\text{O}}_{4}}$、${{\text{H}}_{2}}\text{PO}_{4}^{-}$、$\text{HPO}_{4}^{2-}$、$\text{PO}_{4}^{3-}$的物质的量分数$\delta \left( \text{X} \right)$随$\rm pH$变化如下图所示: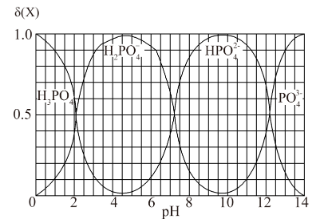 ,由图可知,溶液中磷酸氢根离子浓度和磷酸二氢根离子浓度相等时,溶液$\rm pH$为$\rm 7.2$,由公式可知,电离常数${{K}_{\text{a2}}}\left( {{\text{H}}_{\text{3}}}\text{P}{{\text{O}}_{\text{4}}} \right)=\dfrac{c\left( {{\text{H}}_{\text{2}}}\text{PO}_{\text{4}}^{-} \right)c\text{(}{{\text{H}}^{+}}\text{)}}{c\left( {{\text{H}}_{\text{3}}}\text{PO}_{\text{4}}^{{}} \right)}=c\left( {{\text{H}}^{+}} \right)=1.0\times {{10}^{-7.2}}$,同理可知,电离常数${{K}_{\text{a1}}}\left( {{\text{H}}_{\text{3}}}\text{P}{{\text{O}}_{\text{4}}} \right)=1.0\times {{10}^{-2.2}}$、${{K}_{\text{a3}}}\left( {{\text{H}}_{\text{3}}}\text{P}{{\text{O}}_{\text{4}}} \right)=1.0\times {{10}^{-12.7}}$。
,由图可知,溶液中磷酸氢根离子浓度和磷酸二氢根离子浓度相等时,溶液$\rm pH$为$\rm 7.2$,由公式可知,电离常数${{K}_{\text{a2}}}\left( {{\text{H}}_{\text{3}}}\text{P}{{\text{O}}_{\text{4}}} \right)=\dfrac{c\left( {{\text{H}}_{\text{2}}}\text{PO}_{\text{4}}^{-} \right)c\text{(}{{\text{H}}^{+}}\text{)}}{c\left( {{\text{H}}_{\text{3}}}\text{PO}_{\text{4}}^{{}} \right)}=c\left( {{\text{H}}^{+}} \right)=1.0\times {{10}^{-7.2}}$,同理可知,电离常数${{K}_{\text{a1}}}\left( {{\text{H}}_{\text{3}}}\text{P}{{\text{O}}_{\text{4}}} \right)=1.0\times {{10}^{-2.2}}$、${{K}_{\text{a3}}}\left( {{\text{H}}_{\text{3}}}\text{P}{{\text{O}}_{\text{4}}} \right)=1.0\times {{10}^{-12.7}}$。
$\rm A$.由分析可知,${{K}_{\text{a2}}}\left( {{\text{H}}_{\text{3}}}\text{P}{{\text{O}}_{\text{4}}} \right)=1\times {{10}^{-7.2}}$,则${{K}_{\text{a2}}}\left( {{\text{H}}_{\text{3}}}\text{P}{{\text{O}}_{\text{4}}} \right)$的数量级为$\rm 10^{-8}$,故$\rm A$正确;
$\rm B$.磷酸二氢根离子的水解常数${{K}_{\text{h}}}\text{(}{{\text{H}}_{\text{2}}}\text{PO}_{\text{4}}^{-})=\dfrac{{{K}_{\text{w}}}}{{{K}_{\text{a1}}}}=\dfrac{1.0\times {{10}^{-14}}}{1.0\times {{10}^{-2.2}}}=\rm 1.0\times 10^{-11.8}$,故$\rm B$正确;
$\rm C$.磷酸钠在溶液中的水解程度大于磷酸氢钠,则等体积、等浓度的磷酸钠和磷酸氢钠溶液混合后,磷酸氢根离子浓度大于磷酸根离子浓度,故$\rm C$错误;
$\rm D$.由图可知,溶液$\rm pH$为$\rm 7$时,磷酸二氢根离子浓度大于磷酸氢根离子浓度,故$\rm D$正确;
故选:$\rm C$
高中 | 盐类水解常数题目答案及解析(完整版)
