| 氧化还原反应方程式的书写及配平 题目答案及解析
稿件来源:高途
| 氧化还原反应方程式的书写及配平题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第三节 氧化还原反应
氧化还原反应方程式的书写及配平
三氯化六氨合钴$\rm \left\{ \left[ Co{{(N{{H}_{3}})}_{6}} \right]C{{l}_{3}} \right\}$是一种橙黄色晶体,实验室以活性炭为催化剂,由$\rm CoC{{l}_{2}}$制备三氯化六氨合钴$\rm \left\{ \left[ Co{{(N{{H}_{3}})}_{6}} \right]C{{l}_{3}} \right\}$的实验步骤如下,装置如图所示:
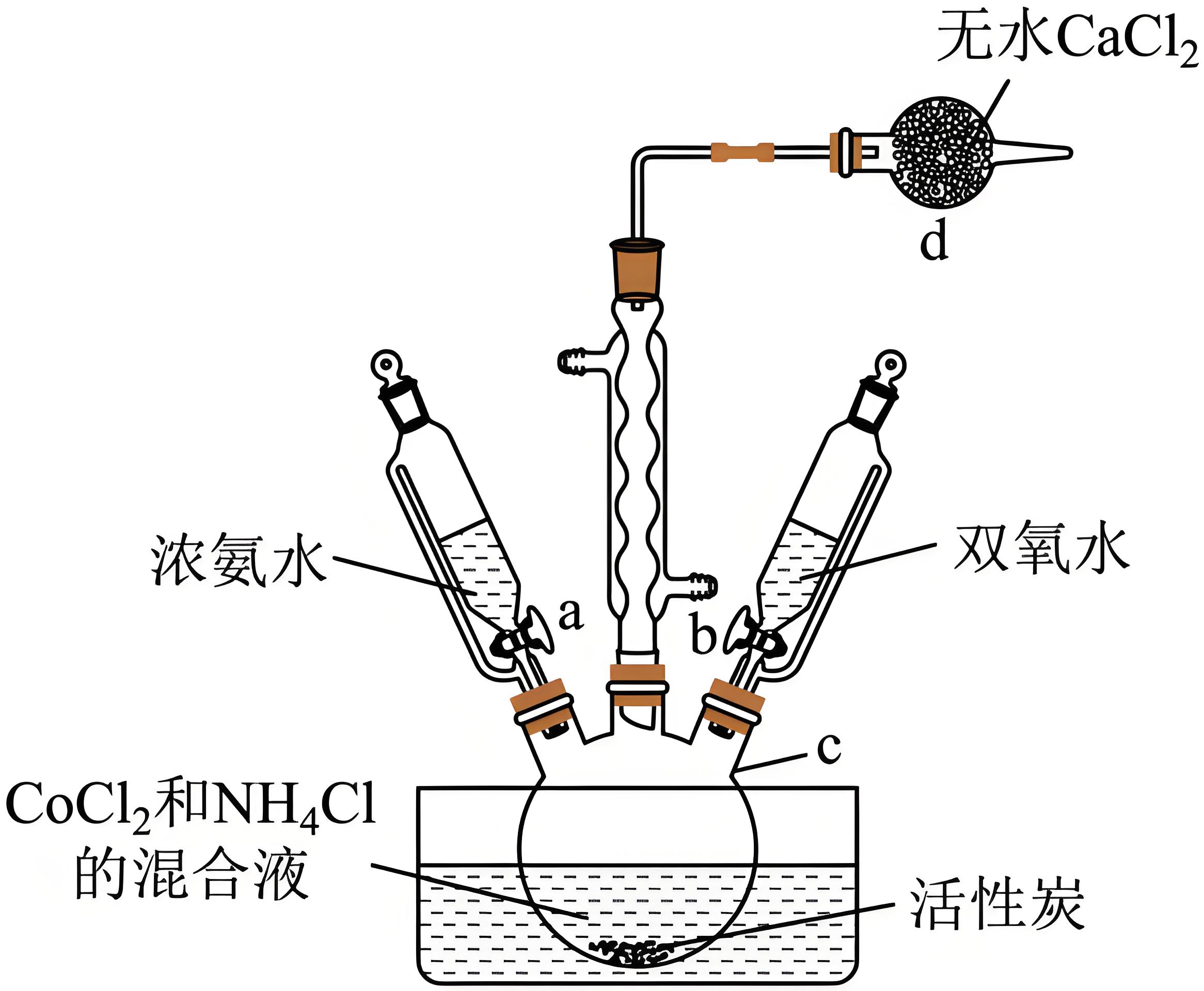
已知:$\rm {{\left[ Co{{(N{{H}_{3}})}_{6}} \right]}^{2+}}$具有较强还原性,$\rm C{{o}^{2+}}$不易被氧化。
步骤$\rm 1$:在三颈烧瓶中加入$\rm CoCl_{2}$和$\rm NH_{4}Cl$的混合液,加入$\rm 0.4$ $\rm g$活性炭,冷却后,先加入$\rm A$溶液充分混合后,再逐滴加入$\rm B$溶液,水浴加热至$\rm 50\sim 60\ ^\circ \text{C}$,保持$\rm 20$ $\rm min$。
步骤$\rm 2$:将所得浊液趁热过滤,向滤液中逐滴加入适量浓盐酸;
步骤$\rm 3$:冷却结晶后抽滤,用少量冷水和无水乙醇分别洗涤晶体$\rm 2\sim 3$次,干燥得到粗产品。
回答下列问题:
仪器$\rm d$的作用是 。
吸收氨气,防止污染空气
"]]该反应中使用了浓氨水,会挥发出氨气,对环境有污染,则仪器$\rm d$的作用是:吸收氨气,防止污染空气;
步骤$\rm 1$中的$\rm A$溶液为 ,$\rm B$溶液为 。
浓氨水 ;双氧水
"]]根据题给信息可知,$\rm {{\left[ Co{{(N{{H}_{3}})}_{6}} \right]}^{2+}}$具有较强还原性,$\rm C{{o}^{2+}}$不易被氧化,则应该先加氨水,将$\rm C{{o}^{2+}}$转化为$\rm {{\left[ Co{{(N{{H}_{3}})}_{6}} \right]}^{2+}}$,即步骤$\rm 1$中的$\rm A$溶液为浓氨水;随后在活性炭做催化剂的条件下,用过氧化氢将$\rm {{\left[ Co{{(N{{H}_{3}})}_{6}} \right]}^{2+}}$氧化为$\rm {{\left[ Co{{(N{{H}_{3}})}_{6}} \right]}^{3+}}$,即$\rm B$溶液为双氧水;
$\rm CoC{{l}_{2}}$制备$\rm \left[ Co{{(N{{H}_{3}})}_{6}} \right]C{{l}_{3}}$的化学方程式为 。
$\\rm 2CoCl_{2}+10NH_{3}\\cdot H_{2}O+H_{2}O_{2}+2NH_{4}Cl\\begin{matrix} \\underline{\\underline{活性炭}} \\\\ {} \\\\ \\end{matrix}2[Co(NH_{3})_{6}]Cl_{3}+12H_{2}O$
"]]由图可知,制备三氯化六氨合钴$\rm ($Ⅲ$\rm )$的反应为氯化亚钴溶液与氯化铵溶液、氨水和过氧化氢溶液反应生成三氯化六氨合钴$\rm ($Ⅲ$\rm )$和水,反应的化学方程式为$\rm 2CoC{{l}_{2}}+10N{{H}_{3}}\cdot {{H}_{2}}O+{{H}_{2}}{{O}_{2}}+2N{{H}_{4}}Cl\begin{matrix} \underline{\underline{活性炭}} \\ {} \\ \end{matrix}2 [ CoN{{H}_{3}}{{}_{6}}] C{{l}_{3}}+12{{H}_{2}}O$;
步骤$\rm 2$趁热过滤的目的是 。
滤去活性炭,避免滤液冷却后析出晶体,降低产率
"]]三氯化六氨合钴$\rm [Co(NH_{3})_{6}]Cl_{3}$易溶于热水,在冷水中溶解度较小,实验室以活性炭为催化剂,来制备产品,故步骤$\rm 2$中趁热过滤的目的是滤去活性炭,避免滤液冷却后析出晶体,降低产率;
步骤$\rm 3$为了得到较大颗粒的$\rm \left[ Co{{(N{{H}_{3}})}_{6}} \right]C{{l}_{3}}$晶体,应该 降温。 如果溶液发生过饱和现象,可采用 、 等方法促进晶体析出。
缓慢; 用玻璃棒摩擦容器内壁 ;加入晶种
"]]晶体颗粒的大小与结晶条件有关,溶质的溶解度越小,或溶液浓度越高,或溶剂的蒸发速度越快,或溶液冷却越快,析出的晶粒就越小,反之可得到较大的晶体颗粒,故为了得到较大颗粒的$\rm \left[ Co{{(N{{H}_{3}})}_{6}} \right]C{{l}_{3}}$晶体,应该缓慢降温;当溶液发生过饱和现象时,振荡容器,用玻璃棒搅动或轻轻地摩擦器壁,或投入几粒晶体$\rm ($晶种$\rm )$,都可促使晶体析出;
抽滤装置如图所示,抽滤完毕,从实验安全角度考虑,首先需进行的操作为 。
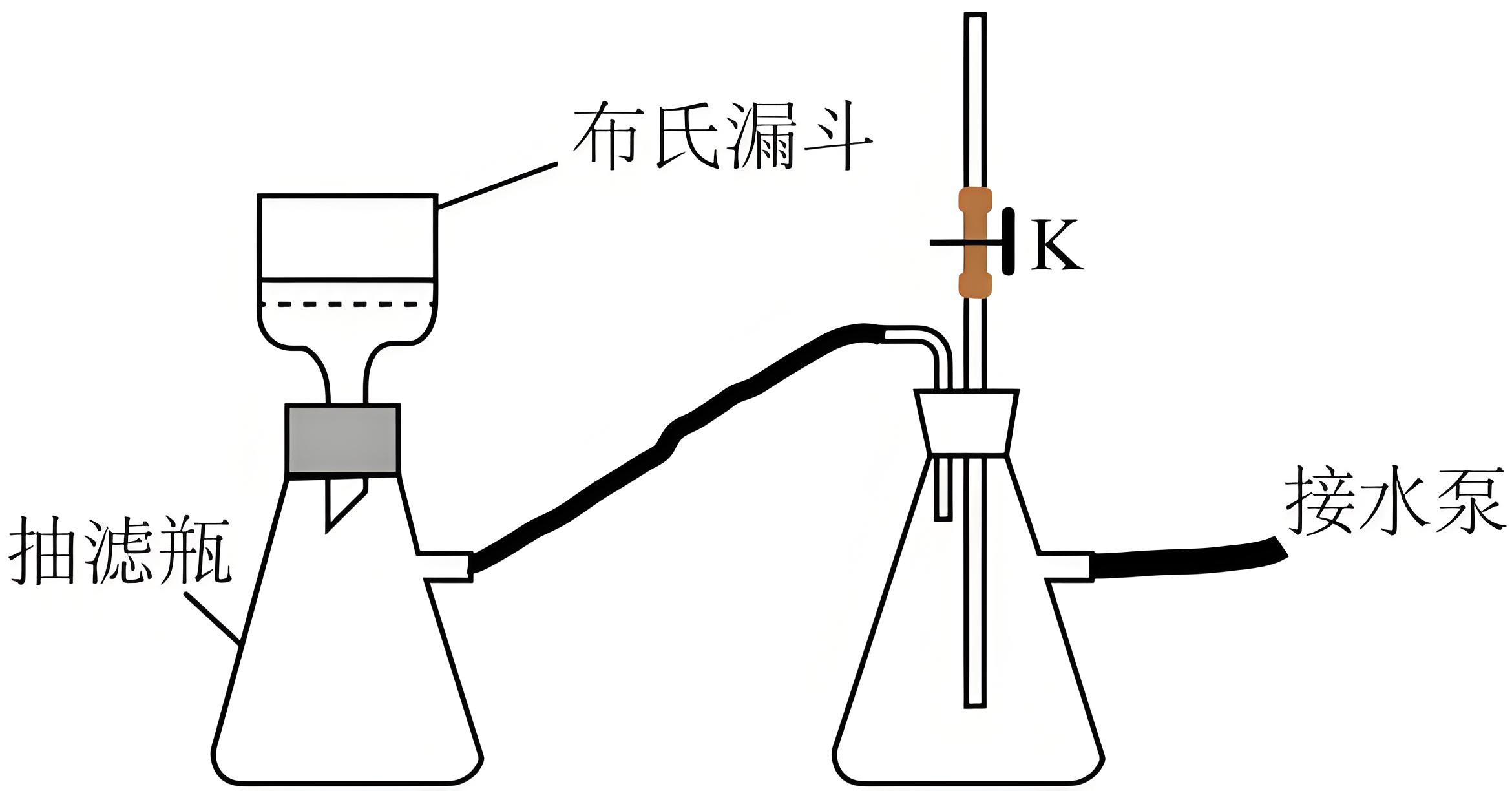
拔下抽滤瓶处橡皮管或打开活塞$\\rm K$
"]]抽滤完毕应首先打开活塞$\rm K$,保持抽滤瓶与外界大气沟通,使内外压强保持平衡,避免有危险发生;
进一步提纯粗产品的方法为 。
重结晶
"]]得到的产品是固体,其中含有杂质,则进一步提纯粗产品的方法为:重结晶。
| 氧化还原反应方程式的书写及配平题目答案及解析(完整版)
