高中 | 化学平衡图像分析 题目答案及解析
稿件来源:高途
高中 | 化学平衡图像分析题目答案及解析如下,仅供参考!
选修四
第二章 化学反应速率和化学平衡
第三节 化学平衡
化学平衡图像分析
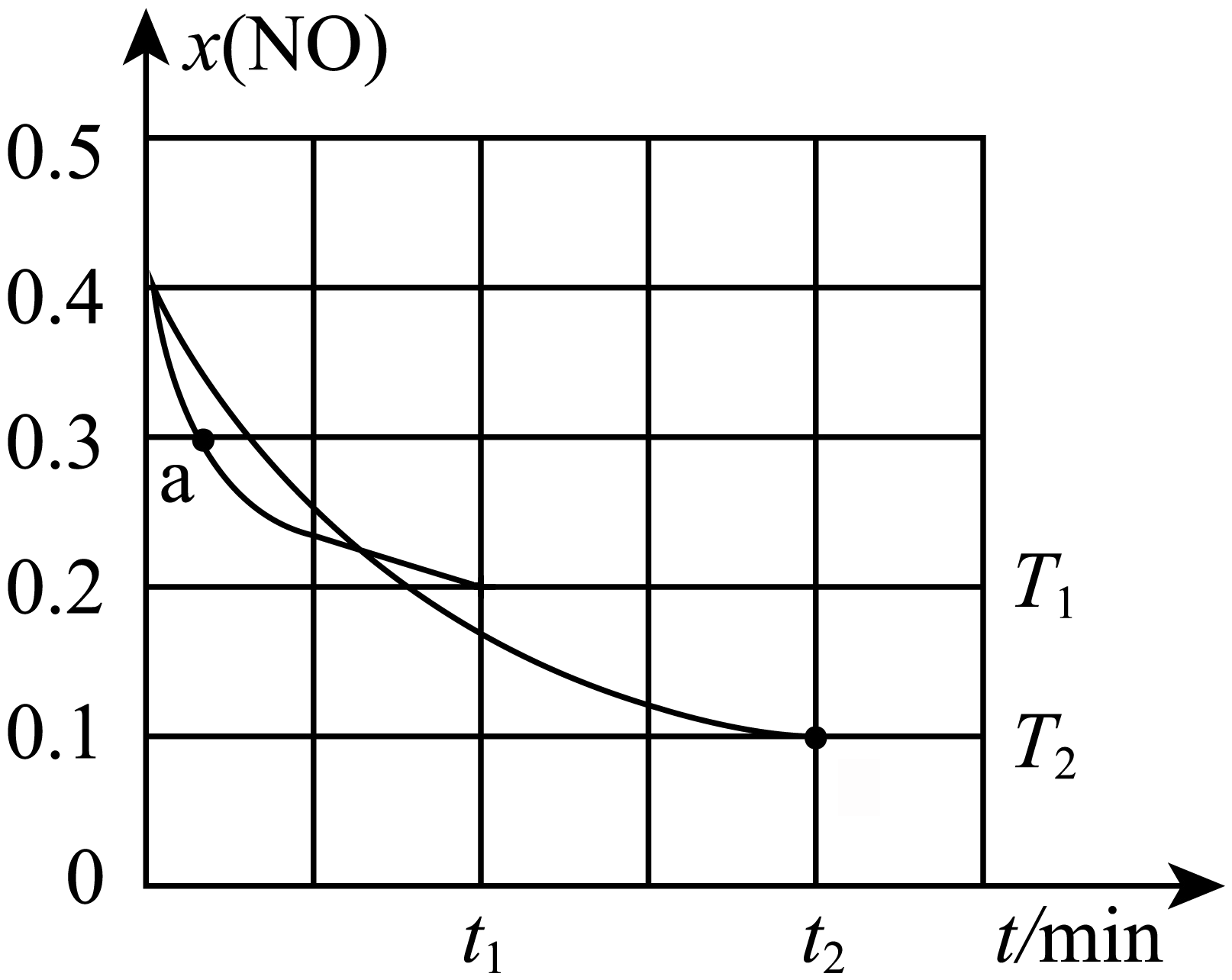
已知基元反应$\rm NO(g)+O_{3}(g)⇌NO_{2}(g)+O_{2}(g)$的速率方程为$v_{正}=k_{正}c\rm(NO)·\textit{c}(O_{3})$、$v_{逆}=k_{逆}c\rm(NO_{2})·\textit{c}(O_{2})$。向$\rm 2\;\rm L$恒容密闭容器中充入$\rm 0.4$ $\rm mol$ $\rm NO(g)$和$\rm 0.6$ $\rm mol$ $\rm O_{3}(g)$发生上述反应,$T_{1}$,$T_{2}$温度时$\rm NO$的体积分数$x\rm(NO)$随时间变化关系如图所示。下列说法错误的是$(\qquad)$
正、逆反应活化能的大小关系为$E_\\rm{a}($正$)\\lt E_\\rm{a}($逆$\\rm )$
","$\\rm a$点:$k_{正}/k_{逆}\\lt[c\\rm(NO_{2})·\\textit{c}(O_{2})]/[\\textit{c}(NO)·\\textit{c}(O_{3})]$
","$T_{2}$温度下,$\\rm O_{3}$的平衡转化率为$\\rm 50\\%$
","温度不变,仅改变初始容器体积,$x\\rm(NO)$随时间的变化曲线不变
"]根据先拐先平数值大可知,$\textit{T}_{1}\gt\textit{T}_{2}$,温度较高的$\rm \textit{T}_{1}$时体积分数$\rm \textit{x}\left( NO\right)$大,说明升高温度平衡逆向移动,逆反应为吸热反应,正反应为放热反应。
$\rm A$.根据先拐先平数值大可知,$\textit{T}_{1}\gt\textit{T}_{2}$,温度较高的$\rm \textit{T}_{1}$时体积分数$\rm \textit{x}\left( NO\right)$大,说明升高温度平衡逆向移动,逆反应为吸热反应,正反应为放热反应,故正、逆反应活化能的大小关系为$E_\rm a\left( 正\right)\lt $$E_\rm a\left(逆 \right)$,$\rm A$正确;
$\rm B$.平衡时${{v}_{正}}={{v}_{逆}}$,$\dfrac{{{\textit{K}}_{正}}}{{{\textit{K}}_{逆}}}=\dfrac{\dfrac{{{\textit{v}}_{正}}}{\textit{c}\left(\rm NO \right)\cdot \textit{c}\left( {{\text{O}}_{3}} \right)}}{\dfrac{{{\textit{v}}_{逆}}}{\text{c}\left(\rm N{{O}_{2}} \right)\cdot \textit{c}\left( {{\text{O}}_{2}} \right)}}=\dfrac{\textit{c}\left(\rm N{{O}_{2}} \right)\cdot \textit{c}\left( {{\text{O}}_{2}} \right)}{\textit{c}\left(\rm NO \right)\cdot \textit{c}\left( {{\text{O}}_{3}} \right)}=\textit{K}\rm $,而$\operatorname{a}$点,反应未达平衡,还在正向移动,此时的${{v}_{正}}\gt {{v}_{逆}}$,代入上式可知,${{\textit{k}}_{正}}/{{\textit{k}}_{逆}}\gt \left[ \textit{c}\left(\rm N{{O}_{2}} \right)\cdot \textit{c}\left( {{\text{O}}_{2}} \right)\left] / \right[\textit{c}\left(\rm NO \right)\cdot \textit{c}\left( {{\text{O}}_{3}} \right) \right]$,$\rm B$错误;
$\rm C$.${{\textit{T}}_{2}}$温度下,平衡时,$\rm NO$占总气体量的$0.1$,由于是等体积反应,反应前后气体的总物质的量不变(均为$\rm 1\ mol$),所以平衡时,剩余的$\rm NO$为$\rm 0.1\ mol$,反应的$\rm NO$是$0.3\rm\ mol$,根据方程式可知,${{\text{O}}_{3}}$反应了$0.3\rm\ mol$,所以${{\text{O}}_{3}}$的平衡转化率为$50\%$,$\rm C$正确;
$\rm D$.温度不变,仅改变初始容器体积,此反应是气体等体积反应,平衡不移动,但是会导致气体浓度改变,化学反应速率变化,$\textit{x}\left(\rm NO \right)$随时间的变化曲线会变,$\rm D$错误;
故选:$\rm BD$
高中 | 化学平衡图像分析题目答案及解析(完整版)
