高中 | 氧化还原反应方程式的书写及配平 题目答案及解析
稿件来源:高途
高中 | 氧化还原反应方程式的书写及配平题目答案及解析如下,仅供参考!
必修一
第二章 化学物质及其变化
第三节 氧化还原反应
氧化还原反应方程式的书写及配平
叠氮化钠$\rm (Na{{N}_{3}})$是一种防腐剂和分析试剂,在有机合成和汽车行业有着重要应用。学习小组对叠氮化钠的制备和产品纯度测定进行相关探究。$\rm ($略去装置图中部分夹持装置$\rm )$
Ⅰ.制备氨基钠的反应为$\rm 2Na+2N{{H}_{3}}\begin{matrix} \underline{\underline{\triangle }} \\ {} \\ \end{matrix}2NaN{{H}_{2}}+{{H}_{2}}$,装置如图。已知:氨基钠$\rm (NaN{{H}_{2}})$的熔点为$\rm 208{\ }^\circ C$,极易与水剧烈反应生成$\rm N{{H}_{3}}$,且易被空气氧化。
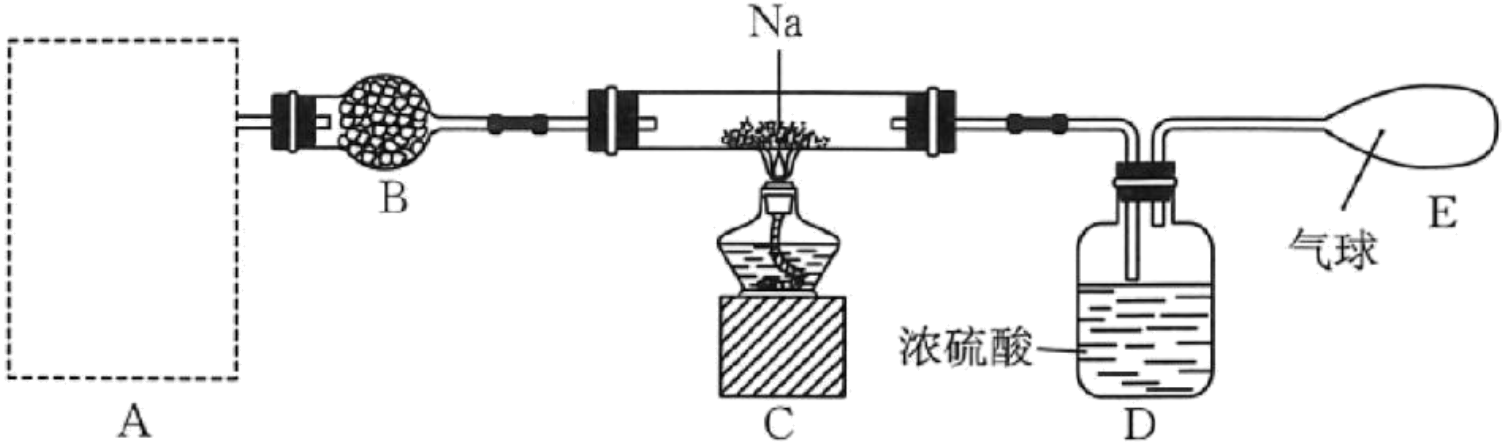
装置$\rm A$为制取氨气的装置,可选择下列装置中的 ;装置$\rm B$中试剂可选用 。
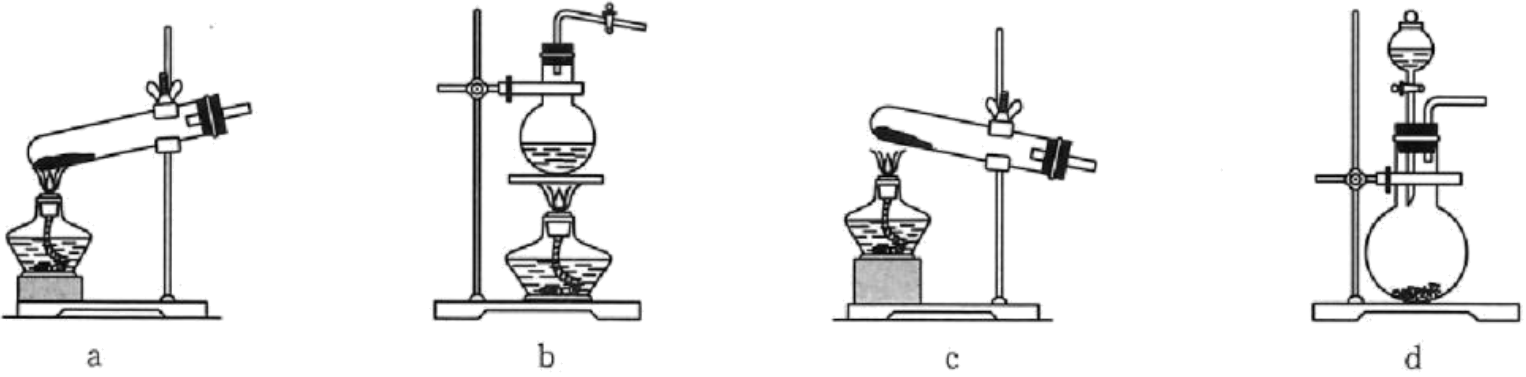
$\\rm bcd$;碱石灰
"]]装置$\rm A$若使用$\rm NH_{4}Cl$和$\rm Ca(OH)_{2}$加热制取氨气,应使用装置$\rm c$,也可使用氨水分解制取氨气方法,即加热浓氨水或将浓氨水滴入固体碱$\rm ($如固体$\rm NaOH$、碱石灰、生石灰$\rm )$,应使用装置$\rm bd$;装置$\rm B$为干燥氨气,应选用碱石灰干燥剂。
Ⅱ.制备叠氮化钠:将得到的$\rm NaN{{H}_{2}}$与在$\rm 210\sim220{\ }^\circ C$的条件下反应生成$\rm Na{{N}_{3}}$、$\rm NaOH$和$\rm N{{H}_{3}}$,反应装置如图$\rm ($装置$\rm C$中温度计略去$\rm )$。已知:有强氧化性,易被还原为$\rm {{N}_{2}}$,不与酸、碱反应。
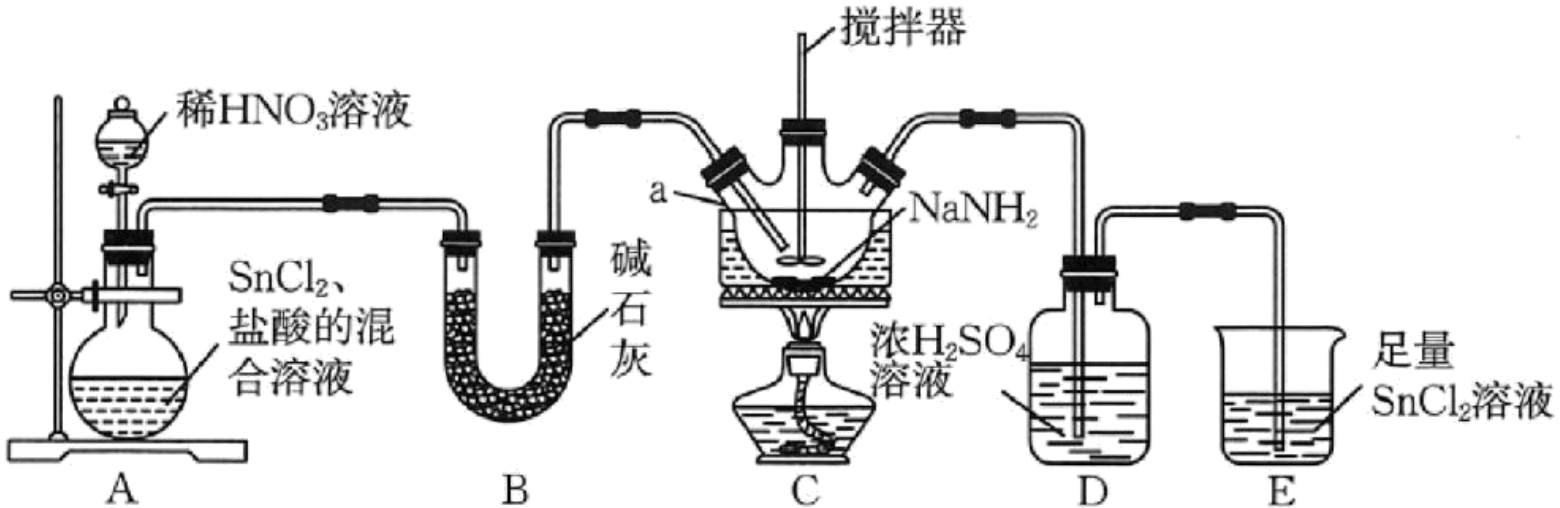
装置$\rm A$用于制备$\rm {{N}_{2}}O$气体,反应中$\rm SnC{{l}_{2}}$生成$\rm SnC{{l}_{4}}$,则该反应中$n{\rm (氧化产物)}:n{\rm (还原产物)}=$ 。
$\\rm 4:1$
"]]装置$\rm A$中发生的反应为$\rm 2HNO_{3}+8HCl+4SnCl_{2}=4SnCl_{4}+5H_{2}O+N_{2}O↑$,$\rm N$元素化合价降低,$\rm HNO_{3}$为氧化剂,$\rm N_{2}O$为还原产物,$\rm Sn$元素化合价升高,$\rm SnCl_{2}$为还原剂,$\rm SnCl_{4}$为氧化产物,则$n{\rm (氧化产物 )}:n{\rm (还原产物 )}=4:1$。
仪器$\rm a$的名称为 ,为了使仪器$\rm a$受热均匀,装置$\rm C$中进行油浴而不用水浴的主要原因是 ,生成$\rm Na{{N}_{3}}$的化学方程式为 。
三颈烧瓶$\\rm ($或三口烧瓶$\\rm )$;反应需要在$\\rm 210\\sim220{\\ }^\\circ C$下进行,水浴加热不能达到该温度;$\\rm 2NaN{{H}_{2}}+{{N}_{2}}O\\begin{matrix} \\underline{\\underline{210\\sim220{\\ \\rm }\\rm ^\\circ C}} \\\\ {} \\\\ \\end{matrix}Na{{N}_{3}}+NaOH+N{{H}_{3}}$
"]]仪器$\rm a$的名称为三颈烧瓶$\rm ($或三口烧瓶$\rm )$;为了使仪器$\rm a$受热均匀,且反应需要在$\rm 210\sim220{\ }^\circ C$下进行,而水浴加热不能达到该温度,因此装置$\rm C$中进行油浴加热;$\rm NaNH_{2}$和$\rm N_{2}O$加热生成$\rm NaN_{3}$、$\rm NaOH$和$\rm NH_{3}$,化学方程式为$\rm 2NaN{{H}_{2}}+{{N}_{2}}O\begin{matrix} \underline{\underline{210\sim220{}\ \rm ^\circ C}} \\ {} \\ \end{matrix}Na{{N}_{3}}+NaOH+N{{H}_{3}}$。
已知装置$\rm E$中生成${\rm Sn{{O}_{2}}}\cdot x\rm {{H}_{2}}O$沉淀,试写出对应反应的离子方程式: 。
${\\rm S{{n}^{2+}}+{{N}_{2}}O}+(x+1){\\rm {{H}_{2}}O=Sn{{O}_{2}}}\\cdot x\\rm {{H}_{2}}O\\downarrow +{{N}_{2}}+2{{H}^{+}}$
"]]装置$\rm E$中$\rm SnCl_{2}$溶液吸收$\rm N_{2}O$生成${\rm Sn{{O}_{2}}}\cdot x\rm {{H}_{2}}O$沉淀,$\rm Sn$元素化合价升高,则$\rm N_{2}O$应被还原为$\rm N_{2}$,对应反应的离子方程式为${\rm S{{n}^{2+}}+{{N}_{2}}O}+(x+1){\rm {{H}_{2}}O=Sn{{O}_{2}}}\cdot x\rm {{H}_{2}}O\downarrow +{{N}_{2}}+2{{H}^{+}}$。
Ⅲ.实验室用滴定法测定某叠氮化钠样品中的质量分数$\rm ($杂质不参与反应$\rm )$:
①将$\rm {1.200\ g}$样品配成$\rm {250.00\ mL}$溶液。
②取$\rm {25.00\ mL}$配成的溶液置于锥形瓶中,用滴定管量取$\rm 25.00\ mL\ 0.1000\ mol\cdot {{L}^{-1}}\ {{(N{{H}_{4}})}_{2}}Ce{{(N{{O}_{3}})}_{6}}$溶液加入锥形瓶中,发生反应$\rm {\left({NH}_{4}\right)_{2} {Ce}\left({NO}_{3}\right)_{6}+{NaN}_{3} \rightarrow {NH}_{4} {NO}_{3}+{Ce}\left({NO}_{3}\right)_{3}+{NaNO}_{3}+{N}_{2} \uparrow}$。
③充分反应后,将溶液酸化,滴入$\rm 3$滴邻菲罗啉指示剂,用$\rm 0.0500\ mol\cdot {{L}^{-1}} \ {{(N{{H}_{4}})}_{2}}Fe{{(S{{O}_{4}})}_{2}}$标准溶液滴定过量的$\rm C{{e}^{4+}}$,消耗溶液的体积为$\rm {14.00\ mL}$,发生反应$\rm {{Ce}^{4+}+{Fe}^{2+} \rightarrow {Ce}^{3+}+{Fe}^{3+}}$。
样品中$\rm Na{{N}_{3}}$的质量分数为 $\rm \%$;若其他操作均正确,下列操作会导致所测样品中$\rm Na{{N}_{3}}$质量分数偏小的是 $\rm ($填标号$\rm )$。
$\rm A$.步骤②中取样品溶液至锥形瓶时,锥形瓶中有少量蒸馏水
$\rm B$.用滴定管量取$\rm {{(N{{H}_{4}})}_{2}}Ce{{(N{{O}_{3}})}_{6}}$溶液,开始时仰视读数,后来俯视读数
$\rm C$.滴定过量的$\rm C{{e}^{4+}}$时,摇动锥形瓶有少量液体溅出
$\rm D$.滴定过量的$\rm C{{e}^{4+}}$时,滴定管开始时尖嘴处有气泡,结束时气泡消失
$\\rm 97.5$;$\\rm BD$
"]]经分析,可知计量关系$\rm Ce^{4+}\sim Fe^{2+}$,$\rm 1.200\ g$样品消耗的$\rm (NH_{4})_{2}Ce(NO_{3})_{6}$的物质的量为$\rm 10\times (25\times 0.1-0.05\times 14)\times {{10}^{-3}}=0.018\ mol$,依据反应,可知$\rm 1.200\ g\ NaN_{3}$的质量为$\rm 65\times 0.018=1.17\ g$,该叠氮化钠样品中$\rm NaN_{3}$的质量分数为$\rm \dfrac{1.17\ g}{1.2\ g}\times 100\%=97.5\%$。
$\rm A$.锥形瓶中残留水不影响滴定结果,不符合题意,故$\rm A$错误。
$\rm B$.滴定过程中开始时仰视读数,后来俯视读数,标准液体积偏小,浓度偏低,$\rm NaN_{3}$质量分数偏小,符合题意,故$\rm B$正确。
$\rm C$.振荡锥形瓶时部分液体溅出,导致滴定测得的$\rm Ce^{4+}$质量减少,原样品中的$\rm Ce^{4+}$质量增加,$\rm NaN_{3}$质量分数偏大,不符合题意,故$\rm C$错误。
$\rm D$.滴定前存在气泡,滴定后气泡消失,标准液体积偏小,浓度偏低,$\rm NaN_{3}$质量分数偏小,符合题意,故$\rm D$正确。
高中 | 氧化还原反应方程式的书写及配平题目答案及解析(完整版)
